Słowa kluczowe: celuloza, błonnik pokarmowy, włókna celulozowe, proces wiskozowy, rozpuszcalność celulozy, odczynnik Schweitzera, odczynnik Cross-Bewana, hydroliza celulozy.Celuloza zwana też błonnikiem jest najbardziej rozpowszechnioną substancją organiczną. Jest ona przede wszystkim budulcem ścian komórkowych roślin , w związku z czym zaliczana jest do tzw. błonnika pokarmowego. Przykładem prawie czystego błonnika jest włókno bawełniane, bibuła bądź wata [2].
Celuloza jest liniowym polimerem β-D-glukopiranozy, a jej podstawową jednostką strukturalną jest celobioza. Tak więc, szereg resz celobiozowych tj. ok. 1500 reszt, tworzy długie łańcuchy, które połączone są siłami międzycząsteczkowymi oraz wiązaniami wodorowymi w równolegle przebiegające pęczki (tzw. micele). To właśnie taka budowa zapewnia celulozie swą dużą wytrzymałość mechaniczną [2].
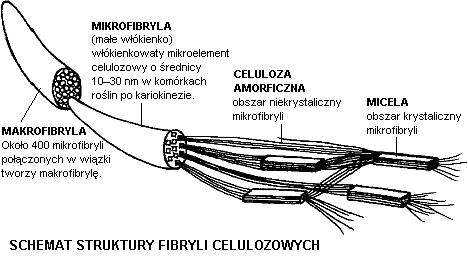 Zdjęcie: http://medycyna.linia.pl/celuloza.html, [4].
Zdjęcie: http://medycyna.linia.pl/celuloza.html, [4].Celulozę budują cząsteczki glukozy, które połąćzone są ze sobą za pomocą wiązania β-1, 4-glikozydowego.
Celuloza jest ciałem stałym o strukturze typowo włóknistej. Jest nierozpuszczalna zarówno w zimnej jak i gorącej wodzie, a ponadto również nierozpuszczalna w rozpuszczalnikach organicznych. Ponadto, charakteryzuje się dużą odpornością na działanie różnych odczynników, w tym na rozcieńczone kwasy. Dopiero bardziej stężone kwasy są w stanie zhydrolizować celulozę. Ponadto, cukier ten rozpuszcza się także w odczynniku Schweitzera lub Cross-Bewana. Co ciekawe, wiele gatunków bakterii, grzybów a także niektóre zwierzęta (np. ślimaki) są zdolne do rozkładania celulozy, a tym samym do korzystania z niej jako pożywienia, a to wszystko dzięki posiadaniu enzymu β-celulazy [2].
Celuloza występuje w zdrewniałych częściach roślin, ziarnach zbóż, nasionach strączkowych, a także warzywach i owocach. Bardzo ważną farkcja celulozy (błonnika) są tzw. polisacharydy mieszane, których bardzo skomplikowaną strukturę tworzą różne cukry proste połączone ze sobą za pomocą wiązań β-glikozydowych [1].
Błonnik pokarmowy, który tworzą cukry oporne na działanie enzymów trawiennych człowieka można w zależności od właściwości podzielić na:
- błonnik rozpuszczalny- tj. węglowodany częściowo przyswajalne degradowane przez drobnoustroje w jelitach m.in. do związków wchłanianych i metabolizowanych w organizmie (np. stachioza, rafinoza, pektyny, hemicelulozy)
- błonnik nierozpuszczalny- czyli tzw. włókno surowe, które oporne jest na działanie enzymów trawiennych i drobnoustrojów (np. celuloza, legnina) [1].
Ponadto, do błonnika zaliczana jest także skrobia oporna, która to nie ma zdolności do kleikowania, w związku z czym nie poddaje się ona działaniu enzymów trawiennych [1].
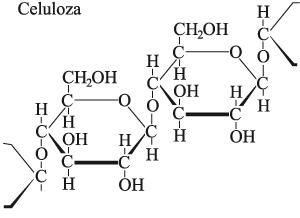 Zdjęcie:Wzór celulozy, http://slownik.ekologia.pl/115_Leksykon_ekologii_i_ochrony_srodowiska/1201_1_C_0_celuloza.html [5].
Zdjęcie:Wzór celulozy, http://slownik.ekologia.pl/115_Leksykon_ekologii_i_ochrony_srodowiska/1201_1_C_0_celuloza.html [5].Nieprzyswajalny błonnik pokarmowy w zależności od udziału frakcji rozpuszczalnej i nierozpuszczalnej, w organizmie człowieka pełni kilka bardzo ważnych funkcji. Między innymi pobudza on funkcję żucia i wydzielania śliny, buforuje oraz wiąże nadmiar kwasu solnego w żołądku , a także ogranicza strawność skłądników odżywczych. Ponadto, błonnik zwiększa wypełnienie jelit, a także pobudza ich ukrwienie i perystaltykę [1].
Jednyną z bardo ważnych cech błonnika jest fakt, że tworzy on korzystne warunki do rozwoju pożądanej flory bakteryjnej w jelitach i zapobiega nadmiernemu odwodnieniu mas kałowych. Powszechnie wiadomo także, że zapobiega on zaparciom oraz zwiększa wydalanie w kale kwasów żółciowych , obniża też stężenie cholesterolu we krwi. Pomimo wielu bardzo ważnych funkcji prozdrowotnych jakie pełni błonnik, należy pamiętać, że spożywanie nadmiernych ilości błonnika nie jest wskazane. A to dlatego, że w nadmiarze może on być przyczyną niedoboru skłądników mineralnych w organizmie [1].
Otrzymywanie włókiem z celulozy drzewnej (w przeciwieństwie do przędzenia bawełny czy lnu) nie jest procesem łatwym, co wynika z konieczności oczyszczania celulozy oraz z faktu jej nierozpuszczalności w większości roztworów i substancji.
Historyczne znaczenie ma tzw. proces miedziowo-amoniakalny odkryty przez Fremery’ego i Urbana w 1897 roku. Polega on na rozpuszczeniu celulozy w roztworze wodorotlenku tetraaminomiedzi (II) (odczynnik Schweitzera, [Cu(NH3)4](OH)2). Proces ten jest mało opłacalny w przemyśle (duże ilości soli miedzi i amoniaku co równa się z kosztownym ich zagospodarowanie), jest jednak najłatwiejszym procesem do prowadzenia w skali laboratoryjnej [3].
Otrzymywanie włókna celulozowegoDo kolby z odczynnikiem Schweitzera należy dodać ok. 3 g celulozy (można stosować watę). Następnie, kolbę zamknąć i wytrząsać aż do momentu rozpuszczenia się celulozy. Po rozpuszczeniu otwartą kolbę wstawić się eksykatora próżniowego i odpowietrzyć roztwór przez ok. 15-20 minut podłączając w tym celu pompę próżniową. W trakcie, gdy roztwór się odpowietrza, w szerokiej zlewce lub krystalizatorze umieścić ok. 200 mL 33% kwasu siarkowego (H2SO4).
Odpowietrzony roztwór celulozy umieścić w strzykawce z igłą i powoli wtłaczać do roztworu kwasu. W trakci ewstrzykiwani abędzie wytrącać się nić, która należy chwycić pęsetą i powoli nawinąć na bagietkę. Po zużyciu całości roztworu celulozy, wypłukać nić kolejno:
- w wodzie,
- 5% roztworze amoniaku
- i wodzie.
Nić (włókno celulozowe) wysuszyć w celu zbadania jego właściwości [3].
Przemysłowe otrzymywanie celulozy- proces wiskozowyDo przemysłowego otrzymywania włókna celulozowego stosowany jest dwuetapowy proces tzw. wiskozowy, który został opracowany w 1892 roku .
W pierwszym kroku tego procesu, celulozę traktuje się ługiem sodowym- w wyniku czego następuje jej częściowa degradacja oraz skrócenie łańcuchów polimeru. Następnie, na tak otrzymaną alkalicelulozę działa się disiarczkiem węgla(IV), co prowadzi do powstania rozpuszczalnego związku zwanego ksantogenianem celulozy. Jego roztwór w rozcieńczonym ługu sodowym stanowi płyn przędzalniczy zwany wiskozą. Wiskoza wtłaczana przez otworki dyszy przędzalniczej do kwaśnej kąpieli zawierającej H2SO4, Na2SO4 i ZnSO4 odtwarza celulozę, która występuje w formie włókien jedwabiu wiskozowego.
Ponadto, poza jedwabiem wizkozowym, celuloza służy także do produkcji celofanu (wizkozę tłoczy się przez szczelinę, a otrzymaną folię nasyca gliceryną, oraz ewentualnie pokrywa wodnoochronną warstwą nitrocelulozy (czyli triazotanem celulozy).
Zaletami procesu wiskozowego jest niski koszt surowca (celuloza drzewna) oraz związków chemicznych (CS2, NaOH, H2SO4). Współcześnie, proces ten z uwagi na uciążliwości środowiskowe , co wiąże się z emisją gazów zawierających siarkę oraz na duże ilości trudnych do oczyszczenia ścieków, jest coraz bardziej problematyczny, a tym samym kosztowny [3].
Badanie rozpuszczalności celulozy1) Badanie rozpuszczalności w odczynniku Schweitzera:
Należy przygotować odczynnik: tj. do 50 ml 0,3M roztworu CuSO4 powoli dolewać, ciągle mieszając 1 M roztwór NaOH, aż do momentu zupełnego wytrącenia się wodorotlenku miedzi (Cu(OH)2) .
Należy unikać nadmiaru wodorotlenku sodu, ponieważ powoduje on czernienie osadu. Otrzymany osad wodorotlenku miedzi przesączyć na sączku, następnie przemyć wodą, na koniec osad zalać 75 ml 28% roztworu amoniaku w parownicy – cały oasad rozetrzeć aż do otrzymania roztworu [2].
2) Do kolby stożkowej (o poj. 250 ml) wsypać 5 g siarczanu miedzi (II), sól rozpuścić w 50 ml wody destylowanej. Następnie , dodawać kroplami 1 M roztwór NaOH (aż do momentu ilościowego wytrącenia wodorotlenku miedzi (Cu(OH)2). Otrzymany osad wodorotlenku odsączyć na lejku, przemyć wodą i wysuszyć w suszarce o temp. 40-50
°C. Tak wysuszony wodorotlenek miedzi przenieść do kolby stożkowej o pojemności 100 ml (z doszlifowanym korkiem), i rozpuścić w wodzie amoniakalnej (w 50 ml). Otrzymany w ten sposób roztwór stanowi odczynnik Schweitzera [3].
W przypadku badania rozpuszczalności celulozy w postaci bibuły lub waty, ciała te podczas wytrząsania w odczynniku Schweitzera powoli się rozpuszczają. Zaś, po zakwaszeniu kwasem solnym, celuloza wytrąca się z roztworu w postaci kłaczków [2].
Badanie rozpuszczalności celulozy w odczynniku Cross-Bewana Należy przygotować odczynnik Cross-Bewana tj. rozpuścić 1 g ZnCl2w 2,5 ml stężonego (37%) roztworu HCl. Celulozę w postaci bibuły lub waty rozpuścić w tym odczynniku, po czym ponownie wytrącić, dodając w tym celu równą objętość wody [2].
Chemicznie czysta celuloza jest białym proszkiem,który całkowicie pozbawiony jest smaku i zapachu. Polisacharyd ten- pomimo dużej polarności jest nierozpuszczalny w wodzie, oraz w większości rozpuszczalników organicznych. Celuloza ulega całkowitej biodegradacji. Biodegradacja zachodzi pod działaniem enzymów celulaz (tj. rozkładających celulozę). Ponadto, ulega także hydrolizie pod działaniem roztworów kwaśnych w podwyższonej temperaturze. Hydroliza zachodzi przez stadium dekstryn (oligomery) do glukozy [3].
Hydroliza celulozy:Celuloza może być zhydrolizowana do glukozy, jednak reakcja ta przebiega znacznie trudniej niż hydroliza skrobi. Wymaga ona obecności stężonego kwasu siarkowego (VI) [H2SO4] oraz długotrwałego ogrzewania. Wskutek hydrolizy celuloza rozpada się na coraz to krótsze łańcuchy dochodząc do stanu końcowego, którym to jest glukoza [2].
Wykonanie:Parę skrawków bibuły należy zalać 10 ml wody oraz dodać 1 ml stężonego roztworu kwasu siarkowego (H2SO4). Tak przygotowaną próbkę wstawić do wrzącej łaźni wodnej na kilkanaście minut. Po inkubacji należy próbkę zobojętnić oraz wykonać próbę redukcyjną na cukry proste [2].
Autor: Lidia KoperwasLiteratura:[1]. Gawęcki J,. Mossor-Pietraszewska T., praca zbiorowa, 2008. Kompendium wiedzy o żywności, żywieniu i zdrowie. Wydawnictwo Naukowe pWN, s. 219-223.
[2]. Kłyszejko-Stefanowicz L, 2003. Ćwiczenia z biochemii. Wydawnictwo Naukowe PWN, 2003, s. 282-283.
[3]. Kacprzak K. Polimery; Wydział Chemii UAM. http://www.poczujchemie.amu.edu.pl/zalaczniki/str/polimery2.0.pdf
[4]. http://medycyna.linia.pl/celuloza.html
[5]. http://slownik.ekologia.pl/115_Leksykon_ekologii_i_ochrony_srodowiska/1201_1_C_0_celuloza.html




Recenzje