Na czym polega profilowanie genetyczne oparte o polimorfizm sekwencji STR?Łańcuch kwasu deoksyrybonukleinowego składa się z sekwencji zasad ułożonych parami tworzących strukturę dwuniciową. Sekwencję DNA można analizować na poziomie pojedynczych nukleotydów. Dzięki technikom biologii molekularnej, takim jak np. reakcja PCR (ang. polymerase chain reaction), możliwa jest analiza zmienności genetycznej [ptaki]. By mówić o polimorfizmie DNA, częstość występowania zmian w sekwencji nukleotydów w danej populacji musi przekraczać 1% [2]. Ponadto, o polimorfizmie genetycznym, w odniesieniu do populacji mówimy, gdy występuje pod postacią minimum dwóch alleli w danym locus. Należy pamiętać, że zmienność ma charakter jakościowy. Co za tym idzie można ją identyfikować za pomocą tak zwanych markerów genetyczny. Polimorfizm można badać w obrębie oraz pomiędzy populacjami. Omawiając analizę polimorfizmu markerów STR należy mieć na uwadze niekodujące fragmenty DNA rozsiane po całym genomie. Locus mikrosatelitarne to sekwencja DNA składająca się z krótkich powtarzających się sekwencji nukleotydów (zwykle w liczbie od 1 do 6 nt). Liczba kopii powtarzalnych elementów jest różna dla poszczególnych alleli. W badaniach najczęściej analizuje się powtórzenia dwu-, trzy, lub czteronukleotydowej [4,5].
W przeciwieństwie do fragmentów polimorficznych DNA, regiony flankujące (okalające) mają charakter konserwatywny (tj. identyczny) wśród osobników tego samego gatunku. Umożliwia to łatwą identyfikację locus mikrosatelitarnego w oparciu o identyfikację regionów flankujących. Markery odznaczające się wysokim stopniem polimorfizmu, głównie loci mikrosatelitarne, umożliwia określenie unikatowego profilu genetycznego człowieka. Do profilowania genetycznego wykorzystuje się różne układy STR (ang. short tandem repeats) dziedziczone po rodzicach [4,6]. Porównanie ze sobą dwóch układów alleli w połączeniu z ich statystyczna analizą pozwala określic stopień pokrewieństwa osobników w populacji, a tym samym np. wykluczyć ojcostwo [4,7].
W wyjątkowych sytuacjach, gdy analiza polimorfizmu mikrosatelitarnych markerów loci STR umiejscowionych na chromosomach automosomalnych jest niewystarczająca, pomocna okazuje się ocena polimorfizmu układów STR chromosomów płci [1,8].
Chromosom Y jest dziedziczony wyłącznie w linii męskiej. W związku z czym, informacje na temat loci Y-STR umożliwia ustalenie spornego ojcostwa, w przypadku gdy np. domniemany ojciec nie żyje (pod warunkiem, że potomstwo jest płci męskiej). Analiza układów STR chromosomu Y, ma nieocenione znaczenie, gdy na podstawie analiz loci STR chromosomów autosomalnych uzyskuje się profil wielokrotny. Taki wynik świadczy o tym, że dany ślad zawiera materiał biologiczny od co najmniej dwóch osób. Wyjątkowo trudny materiał do analizy genetycznej stanowi wymaz z dróg rodnych kobiety w przypadku gwałtu zbiorowego. Wówczas na zabezpieczonej „wymazówce” znajduje się mieszanina DNA kobiety i mężczyzn. Na podstawie wyników można określić liczbę sprawców. A porównując z pojedynczymi profilami genetycznymi próbek pobranych od podejrzanych mężczyzn, metoda ta pozwala na jednoznaczne wskazanie lub wykluczenie sprawców przestępstwa [8].
Analogicznie do analizy układów STR znajdujących się na chromosomie Y, określenie loci STR umiejscowionych na chromosomie X umożliwia ustalenie stopnia pokrewieństwa w linii żeńskiej np. sióstr, a także ojcostwa w przypadku, gdy spór dotyczy córki. Dziecko może zostać poddane badaniu nawet, gdy ojciec z różnych przyczyn jest nieobecny. Wówczas można uznać lub wykluczyć ojcostwo, na podstawie porównania materiału genetycznego małoletniej z materiałem genetycznym matki domniemanego ojca (babki małoletniej powódki). Analiza polimorficznych sekwencji chromosomu X może stanowić dodatkowy dowód w przypadku zgwałcenia. Markery oznaczone na chromosomie X poszkodowanej kobiety pozostawione na odzieży lub ciele sprawcy mają inne allele, niż ofiara loci chromosomu X poddawanych analizie [1].
Wyniki badań populacyjnych wskazują na duże zróżnicowanie genetyczne w obrębie badanych układów STR wśród ludzi. Wyniki badań umożliwiają określenie prawdopodobieństwa wystąpienia się tego samego profilu genetycznego u dwóch osobników w kontekście częstości występowania danych alleli określonego układu STR. Wyniki analiz biostatystycznych wskazują na zasadność ustalania i porównywania profili genetycznych na potrzeby ekspertyz medyczno-sądowych [2,4].
Badając układy STR genomowego DNA można określić zmienność genetyczną na poziomie populacji. Krótkie powtórzenia repetytywne niosą informację o charakterze diploidalnym (2n). Natomiast, do analizy zmienności genetycznej na poziomie gatunków częściej wykorzystuje się mitochondrialne DNA (mtDNA). Badając mtDNA uzyskujemy informacje o charakterze haploidalnym (1n). Różnice te wynikają z odmiennego sposobu dziedziczenia DNA genomowego i mitochondrialnego[9].
Analiza ludzkiego mtDNAW sytuacji, gdy oznaczenie profilu genetycznego na podstawie układów STR chromosomów autosomalnych, czy też płci jest niemożliwe, z pomocą przychodzi technika oparta o sekwencjonowanie DNA pochodzenia mitochondrialnego. W kryminalistyce od lat z powodzeniem stosuje się rutynowo analizę mtDNA do badania śladów biologicznych o wysokim stopniu degradacji DNA jądrowego. Kości, zęby, a także trzony włosów (które poza cebulką nie zawierają jądrowego DNA), ze względu na swój charakter stanowią trudny materiał do badań genetycznych. Do ich analizy zazwyczaj również stosuje się techniki molekularne prowadzące do uzyskania profilu mtDNA [9].
Budowa mtDNA różni się znacznie od struktury DNA jądrowego. MtDNA posiada kolistą strukturę i przyjmuje konformację superskręcona, co zapewnia wyższą odporność na degradację w stosunku do DNA jądrowego. Mitochondrialne DNA zawiera wyłącznie sekwencje kodujące (eksony) i w żaden sposób nie jest związane z białkami histonowymi. Jak sama nazwa wskazuje znajduję się w jednym z organelli komórkowych, a mianowicie w mitochondriom, czyli w centrum energetycznym komórki [9].
Kolejną cechą odróżniającą mtDNA od DNA jądrowego jest częstość występowania mutacji. W mitochondriach obserwuje się wysokie stężenie wolnych rodników, które powstają w trakcie przemieszczania się elektronów przez łańcuch oddechowy. Ponieważ DNA mitochondrialne nie posiada osłony w postaci białek histonowych, bardzo łatwo ulega atakom wolnych rodników, w wyniku czego dochodzi do zmian w materiale genetycznym. Poza tym same mechanizmy naprawcze funkcjonują z mniejszą skutecznie, niż w jądrach komórkowych. Wszystko to ma wpływ na większe tempo ewolucji mtDNA względem DNA jądrowego (od 5 do10 razy szybciej). W celu ustalenia profilu genetycznego mtDNA ludzi zastosowanie znalazły dwa regiony hiperzmienne: HV1 oraz HV2. Regiony te położone są w jedynym fragmencie mtDNA, który pozbawiony jest genów, w obrębie tak zwanego punktu kontrolnego. Punkt ten stanowi pętla D (ang. D-loop), która de facto stanowi miejsce inicjacji transkrypcji. Region kontrolny zajmuje około 7% całego genomu mtDNA i ma długość około 1100 par zasad. Zazwyczaj HV2 lokuje się na odcinku od 73 do 340 pary zasad, a HV1 od 16024 do 16365 pary zasad. Przełomowym momentem w analizach mtDNA było zsekwencjonowanie całego genomu mitochondrialnego przez Andersona i jego współpracowników w 1981 roku [9,10]. Na cześć badacza sekwencja ta nazwana jest sekwencją referencyjna Andersona (inaczej Sekwencja Referencyjna z Cambridge – CRS, ang. Cambridge Reference Sequence). Do CRS jako standardu odnosi się wszystkie nowo zsekwencjonowane haplptypy. Pdając wynik z badań w ekspertyzach kryminalistycznych podaje się jedynie pozycje nukleotydów którymi uzyskany profil różni się od Sekwencji Referencyjnej [9].
W metodyce badawczej, do analizy mtDNA standardowo wykorzystuje się reakcję sekwencjonowania. Specyfika tej techniki wymaga dużej uwagi pod kątem niwelowania możliwości pojawienia się problemu jakim jest kontaminacja próbek obcym DNA. Monitorowane badanych próbek pod kątem wystąpienia zanieczyszczeń, polega na stosowaniu kontroli negatywnej i pozytywnej zarówno procesu amplifikacji jak i samej ekstrakcji materiału genetycznego. Zafałszowania wyniku w próbkach zawierających domieszkowe DNA można uniknąć dopóki dodatkowy materiał genetyczny stanowi mniej niż 10% badanej próbki [9].
Człowiek, zwierze czy roślina - czyli barkoding DNARobiąc na co dzień zakupy, nikogo nie dziwi obecność kodów paskowych na opakowaniu każdego artykułu. Kod ten zawiera szereg informacji, które można odczytać za pomocą odpowiedniego aparatu. Od pewnego czasu, w świecie nauki, zaczęto odnosić kody paskowe do sekwencji DNA organizmów żywych. Jak wynika z informacji zawartych w pierwszej części niniejszej publikacji, na podstawie sekwencji nukleotydowej możliwa jest identyfikacja genetyczna poszczególnych osobników w obrębie populacji z określeniem przynależności gatunkowej. Czy podjęta inicjatywa utworzenia ogromnej biblioteki, w której będą się znajdowały katalogi wszystkich gatunków organizmów żyjących na Ziemi jest możliwa? Na pewno stanowi ogromne wyzwanie wynikające z wielu ograniczeń, ale wbrew pozorom może jest możliwa do zrealizowania. Po pierwsze do identyfikacji należy wybrać taki obszar DNA, który będzie powtarzalny u osobników tego samego gatunku i jednocześnie unikatowy na poziomie międzygatunkowym. Stworzenie „kodu paskowego DNA” musiałoby polegać na określeniu specyficznej dla danego gatunku kolejności nukleotydów w danym locus [3].
Samo sformułowanie barkoding DNA (ang. DNA barcoding) określa cały proces wraz ze stosowanymi technikami zmierzające do ustalenia „kodu paskowego DNA”. Określenia tego używa mając na myśli poziom gatunkowy. Natomiast, barkod DNA (ang. DNA barcode) to sama sekwencja DNA, która znajduje się w wybranym standardowym regionie genomu, umożliwiająca identyfikację gatunku. Herbert i wsp. [11] w swoich badaniach zmierzających do wytypowania locus przydatnego do rozróżniania gatunków zwierząt, wytypowali mitochondrialną sekwencję I genu oksydazy cytochromowej (cox1, CO1) [3].
Analogicznie do odczytywania kodów paskowych w sklepach przy zakupie towaru, barkoding DNA powinien być: łatwy w obsłudze, szybki, wystandaryzowany w skali globalnej oraz wiarygodny. Ponadto, urządzenie do sekwencjonowania powinno być w miarę tanie i wygodne w użyciu.
Idea barkodów DNA niesie ze sobą ich praktyczne zastosowanie, np. do:
• opisu i ewidencjonowania bioróżnorodności,
• przeprowadzania analiz ekologicznych i fitogeograficznych,
• analiz kryminalistycznych w celu wydawania pełniejszych ekspertyz,
• ustalania składu żywności oraz leków,
• kontroli „bezpieczeństwa biologicznego”,
• zapobieganiu lub identyfikowaniu nielegalnego handlu zwierzętami lub roślinami będących pod ochroną,
• klasyfikacji i opisywania nowych gatunków [3].
Z wyników publikowanych prac wynika, że tylko pojedyncze obszary genomu nadają się do wykorzystania jako barkody DNA. Idealny „kod paskowy DNA” powinien charakteryzować się następującymi cechami:
- wysoką zmiennością międzygatunkową i jednocześnie niską zmiennością wewnątrzgatunkową (około 2%),
- konserwatywnymi domenami flankującymi, umożliwiającymi zaprojektowanie starterów do reakcji PCR poprzedzającej sekwencjonowanie,
- niewielka długością, w granicach około 600 par zasad,
- nie powinny zawierać mutacji powstałych w wyniku insercji lub delecji, natomiast mile widziane są substytucje, obecność dużej liczy ich kopii w genomie [3].
W przypadku barkodingu DNA roślin, wykorzystywana standardowo dla zwierząt sekwencja cox1 u roślin lądowych nie cechuje się wystarczającą zmiennością [Kress+bar], w związku z czym nadaje się jedynie do scharakteryzowania wyłącznie niektórych grup glonów [Saunders 2005 + bar]. Ponieważ w mtDNA roślin następują częste rearanżacje, a także wymiana genów z DNA jądrowym, nie stanowi przydatnego źródła sekwencji do barkodingu DNA [bar]. Podobnie jak w przypadku grzybów, zalecanymi dla roślin, jako standard do barkodingu ich DNA początkowo wskazywano ITS ( ang. internal transcribed spacer), czyli niekodująca domenę, która występuje w obrębie genów rybosomalnego DNA (rDNA). O wiele lepszą alternatywą, do identyfikacji genetycznej roślin okazała się byś analiza chloroplastowego DNA (cpDNA). Zaleta cudna jest to, że występuje w komórkach roślinnych w wielu kopiach. Sekwencje kodujące cpDNA wykazują nieznaczną zmienność, natomiast sekwencje niekodujące relatywnie dużą. Standardowo proponowane są dwa zestawy sekwencji, zawierające po trzy regiony chloroplastowego DNA:
1. rpoC1, matK, rpoB;
2. rpoC1, matK, trnH – psbA.
Na dzień dzisiejszy nie ma jednoznacznej odpowiedzi, który zestaw sekwencji bardziej przydaje się do tworzenia bar kodów. Grupa genów rpoC1, matK, rpoB – zawiera wyłącznie regiony kodujące. Z kolei w skład drugiej sekwencji genów wchodzi jena domena niekodująca, a mianowicie: trnH – psbA. Aby jednoznacznie wskazać „zwycięzcę” niezbędne są dalsze badania [3,12].
W pracy opublikowanej w 2006 roku Newmaster i współpracownicy [13], zaproponowano by identyfikacji genetycznej dokonywać dwuetapowo. W pierwszej kolejności należy analizować sekwencję „pierwszorzędową”, umożliwiającą wskazanie wyższej jednostki systematycznej, takiej jak: rząd, rodzina, czy rodzaj. Następnie w drugiej turze badań, na podstawie sekwencji „drugorzędowej” możliwe jest określenie przynależności gatunkowej identyfikowanego okazu [3].
Pomysł Newmastera i wsp. spodobał się badaczom Kress i Erickson [14], na tyle, że postanowili go rozwinąć. Do oceny przydatności dziewięciu potencjalnie przydatnych sekwencji w barkodingu DNA zastosowali dwa kryteria. Po pierwsze, na podstawie danej sekwencji DNA ważna jest możliwość różnicowania gatunków. Po drugie, od strony technicznej, wybrany gen lub geny powinny ulegać uniwersalnej amplifikacji, czyli za pomocą uniwersalnych starterów znajdujących się w mixie reakcyjnym PCR powinny zostać powielone. Analizom poddano następujące geny: trnH – psbA, rbcL-a, ITS1,accD, matK, rpoB2, rpoC1, ycf5, ndhJ. Okazało się, że sekwencje rpoB2, rpoC1 ulegają uniwersalnej amplifikacji, ale nie spełniają w pełni pierwszego kryterium, wykazując zbyt niski poziom różnicowania osobników miedzy gatunkami. Z kolei wyniki prac nad analizą genu matK dały zadowalający rezultat pod względem różnicowania gatunków, natomiast słabą stroną wybranej metody okazała się być możliwości amplifikacji. W tym wypadku należałoby zwiększyć uniwersalność powielania fragmentu matK, poprzez opracowanie odpowiedniej pary starterów. Wytypowano dwie sekwencje, które najlepiej spełniają oba wymagane kryteria. Pierwsza z nich to gen rbcL-a, który umożliwia z wysokim stopniem prawdopodobieństwa przyporządkować dany okaz do rodzaju lub rodziny. Druga sekwencja, czyli trnH-psbA pozwala na identyfikacje gatunków w obrębie wymienionych grup[3].
Przedstawione powyżej przykłady wskazują na to, iż nie da się zastosować wyłącznie jednej sekwencji DNA do opracowania uniwersalnej procedury barkodingu DNA. Poza tym należy pamiętać, że zarówno cpDNA jak i mtDNA przekazywane jest w linii żeńskiej. Co za tym idzie, odróżnianie gatunków mieszańcowych może być utrudnione. Ma to istotne znaczenie zwłaszcza w przypadku roślin, pod kątem analizy DNA pochodzenia chloroplastowego u gatunków aloploidalnych [3].
Zamiast podsumowania – bazy DNA Działania zmierzające do identyfikacji osobników na podstawie ich profili genetycznych, pociągają za sobą konieczność tworzenie baz lub bibliotek genowych. W celu klasyfikacji gatunków opartych o barkody DNA podjęto inicjatywę utworzenia bazy danych BOLD (ang. Barcode of Life Data System), która zawiera w swych archiwach ponad 39 000 gatunków opatrzonych barkodem DNA. Biblioteka ta zawiera z zarówno dane o charakterze molekularnym, jak i dane opisy związane z tradycyjna taksonomią głównie zwierząt. Do tej pory rośliny nie „doczekały” się swojej osobnej bazy, nie posiadają też wyodrębnionej części bazy BOLD. Informacje dotyczące roślin zamieszcza się w bazach o przeznaczeniu ogólnym, do których należy np.: GenBank [3].
Oczywiście swoje bazy posiadają również takie jednostki jak FBI. Jako przykład można podać bazę stworzoną przez SWGDAM, czyli Grupę Roboczą ds. Metod Analizy DNA. W bazie tej są gromadzone informacje na podstawie danych zebranych w wyniku analizy mtDNA [9].
Autor: Agnieszka GudekLiteratura:
1. Cybulska L., Szczerkowska Z., Wysocka J., Rębała K. Polimorfizm chromosomu X – STR loci DXS7108 i DXS1196 w populacji Polski Północnej. ARCH. MED. SĄD. KRYM. 2005; LV: 32-35.
2. Czarny M., Kwiatkowska J., Słomska M., Siemieniako B., Słomski R. Możliwości badawcze polimorficznych loci DNA człowieka i ich wykorzystanie w badaniach medyczno-sądowych. ARCH. MED. SĄD. KRYM. 1995; XLV: 3-4, 259-269.
3. Mirek Z., Bieniek W., Sztorc A. Barkoding DNA – nowe narzędzie do opisu bioróżnorodności. Wiadomości Botaniczne 2007; 51(3/4): 41–50.
4. Zagalska-Neubauer M., Dubiec A. Techniki i markery molekularne w badaniach zmienności genetycznej ptaków. Notatki ornitologiczne 2007; 48: 193-206.
5. Li Y.C., Korol A.B., Fahima T., Beiles A., Nevo E. 2002. Microsatellites: genomic distribution, putative functions, and mutational mechanisms: a review. Mol. Ecol. 11: 2453–2465.
6. Queller D.C., Strassmann J.E., Hughes C.R. 1993. Microsatellites and kinship. Trends Ecol. Evol. 8: 285–288.
7. Blouin M.S. 2003. DNA-based methods for pedigree reconstruction and kinship analysis in natural populations. Trends Ecol. Evol. 18: 503–511.
8. Janica J., Pepiński W., Niemcunowicz-Janica A., Skarwońska M., Sołtyszwski I., Berent. Polimorfizm loci Y-STR wśród ludności Polski północno-wschodniej w aspektach zróżnicowania etnicznego i przydatności w badaniach medyczno-sądowych. ARCH. MED. SĄD. KRYM. 2008; LVIII: 12-21.
9. Gawęda-Walerych K., Sołtyszewski I. Zastosowanie analizy mitochondrialnego DNA w badaniach kryminalistycznych – perspektywy. Problemy kryminalistyki 2005; 248/05:5-13.
10. Anderson S., Bankier A., Barrel B., de Bruijn M., Coulson A., Drouin J., Eperon I., Nierlich D., Roe B., Sanger F., Schreier P., Smith A., Staden R., Young I. Sequence and organization of the humane mitochondrial genome. Nature 1981; 290: 457-465.
11. Herbert P. D. N., Cywinska A., Ball S. L., Dewaard J. R.. Biological identifications through DNA barcodes. Proc. R. Soc. Lond. B. Biol. Sci. 2003a; 270: 313–321.
12. Chase M. W., Salamin N., Wilkinson M., Dunwell J. M., Kesanakurth R. P., Haidar N., Savalainen V.. Land plants and DNA barcodes: short-term and long-term goals. Phil. Trans. R. Soc. 2005; B 360 (1462): 1889–1895.
13. Newmaster S. G., Fazekas A. J., Ragupathy S. DNA barcoding in land plants: evaluation of rbcL in a multigene tiered approach. Can. J. Bot 2006. 84: 335–341.
14. Kress W. J., Erickson D. L.. A two-locus global DNA barcode for land plants: the coding rbcL gene complements the non-coding trnH-psbA spacer region. PLOS One 2007; 6 (e508): 1–10.


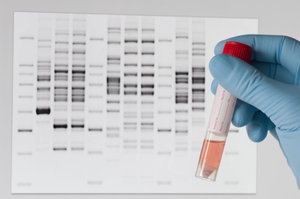 Pytając na ulicy przypadkowego przechodnia o to, z czym kojarzy mu się pojęcie „identyfikacji genetycznej”, najprawdopodobniej uzyskamy odpowiedź, że z ustalaniem sprawców przestępstw. Jest to jak najbardziej słuszne twierdzenie, ale nie określa w pełni zakresu badań jakie przeprowadza się w laboratoriach genetycznych.
Pytając na ulicy przypadkowego przechodnia o to, z czym kojarzy mu się pojęcie „identyfikacji genetycznej”, najprawdopodobniej uzyskamy odpowiedź, że z ustalaniem sprawców przestępstw. Jest to jak najbardziej słuszne twierdzenie, ale nie określa w pełni zakresu badań jakie przeprowadza się w laboratoriach genetycznych.
Recenzje