Rysunek 1. Dystrybucja w organizmie i istota działania radiofarmaceutyków terapeutycznych oraz diagnostycznych. Na rysunku: wiązanie niespecyficzne (ang. non-specific sites), nerki (ang. kidneys), wątroba (liver), nowotwór (ang. tumor), wciągnięcie do środka (ang. internalization), radioizotop (ang. radioisotope), peptydowy nośnik radioizotopu (ang. peptide analog), receptor (ang. receptor), komórka nowotworowa (ang. tumor cell), terapia (ang. therapy), diagnostyka (ang. diagnosis), komórka sąsiadująca (ang. neighboring cell) [1].
Radioizotop technetu-99mTechnet-99m należy do siódmej grupy układu okresowego. 99mTc (t1/2 = 6,01 h) jest metastabilnym izotopów promieniotwórczych emitującym promieniowanie gamma (fotony) o energii 143 keV. Radioizotop ten rozpada się na bardzo stabilnych siostrzany izotop 99Tc. Czas półtrwania izotopu technetu-99m (t1/2 = 6,01 h) jest wystarczający do właściwego przygotowania procedury skanowania radiofarmaceutyku SPECT i jest na tyle krótki, by zachować na niskim poziomie całkowitą dawkę jaką przyjmuje pacjent podczas ekspozycji. 99mTc otrzymywany jest w postaci jonów 99mTcO4- z generatora radionuklidów 99Mo/99mTc. Wyjściowy radionuklid generatora technetu-99m, którym jest molibden-99 (t1/2 = 2,78 dni) stanowi produkt rozszczepienia uranu-235. W generatorze 99Mo/99mTc, jony 99mTcO4- są tworzone w wyniku rozpadu 99MoO42-. 99mTcO4- (wysoka aktywność właściwa) wymywany jest z kolumny chromatograficznej połączonej z generatorem za pomocą soli fizjologicznej. Całkowite stężenie technetu w eluencie generatorowym 99Mo/99mTc zawiera się w zakresie 10-7 - 10-6 molxL-1.
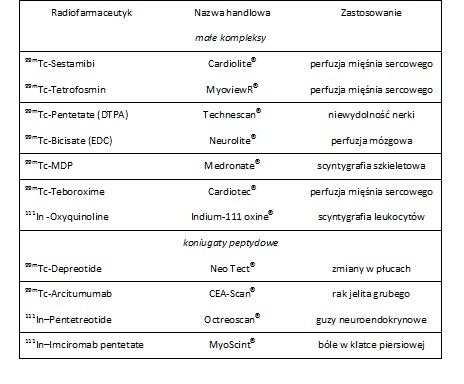
Ze względu na krótki okres półtrwania, większość radiofarmaceutyków opartych na 99mTc jest prostymi kompleksami metalu lub koniugatami metalu z krótkimi peptydami lub białkami.
Historycznie pierwszy generator 99Mo/99mTc został opracowany w latach pięćdziesiątych XX wieku przez Brookhaven National Laboratory, który zrewolucjonizował badania radiofarmaceutyczne opierające się na 99mTc Badania zostały przyspieszone, aby w latach osiemdziesiątych kupić się głównie na produkcji małych kompleksów 99mTc jako radioznaczników perfuzji serca i mózgu. Szeroko zakrojone badania koordynacyjnej chemii technetu-99m doprowadziły do pomyślnego rozwoju wielu nośników 99mTc pierwszej generacji, które są znane jako podstawowe czynniki technetu.
W 1981 roku odkryto jeden z najbardziej istotnych podstawowych czynników 99mTc, o nazwie [99mTc (MIBI)6]+ (MIBI: 2-metoksy-2-metylpropylisonitryl), który gromadził się w tkankach sercowych po podaniu dożylnym. Związek ten znany jest pod nazwą handlową Cardiolite lub Sestamibi. Otrzymany koniugat pomaga w ocenie ilości krwi przepływającej przez mięsień sercowy w warunkach spoczynku oraz stresu. Wykorzystanie koniugatu jest szerokie, gdyż można go podać zarówno ludziom, którzy już mają objawy ataku serca, ale również ludziom, którzy są w grupie ryzyka, lecz nie wykazali oznak. Prócz Sestamibi dostępny jest w handlu inny środek obrazowania perfuzji mięśnia sercowego, a mianowicie 99mTc-Tetrofosmin o nazwie [99mTcO2(tetrofosmin)2]+ (tetrofosmin: 1,2-bis[bis(2-etoksyetylo)fosfinoetan) (Tab. 1).
Radioizotop galu-67Gal-67 występuje w postaci silnie kwaśnych kationów na plus trzecim stopniu utlenienia (67Ga3+). Gal-67 korzystnie wiąże się z chelatorami zawierającymi anionowe grupy funkcyjne (DFO, DOTA, DTPA). Radionuklid wytwarzany jest w cyklotronie metodą protonowego bombardowania natywnej tarczy cynkowej (natZn). Produkcja izotopu 67Ga trwa w granicach 15-20 godzin. Radionuklid o wysokiej czystości izolowany jest z tarczy przez rozpuszczenie i chromatografię z wykorzystaniem organicznych żywic polimerowych zawierających groupy niewymienne z jonami.
67Ga (t1/2 = 78,3 h) rozpada się na stabilny 67Zn przez wychwytywania elektronów (ang. elektron capture) i jest szeroko stosowany w medycynie jądrowej. Chociaż koniugat 67Ga(III) z cytrynianem nie jest związkiem specyficznym dla konkretnego nowotworu, to koncentruje się w wielu typach guzów i niezłośliwych zmianach chorobowych, zwłaszcza zapalnych.
Ogólnie rzecz biorąc, 67Ga(III)-cytrynian wiąże w osoczu krwi transferyny i następnie transportowany jest do tkanek nowotworowych.
Przy zastosowaniach immunologicznych SPECT, 67Ga skoniugowany jest z przeciwciałami monoklonalnymi poprzez desferoksyaminę (DFO) lub kwas 1,4,7,10-tetraazacyklododekano-1,4,7,10-tetraoctowy (DOTA) bez utraty zdolności wiązania antygenu (Rys. 6).

Rysunek 6. Struktury przestrzenne chelatorów dwufunkcyjnych stosowanych w SPECT. Na rysunku: NOTA - kwas 1,4,7-triazacyklononano-1,4,7-trioctowy, DOTA - kwas 1,4,7,10-tetraazacyklododekano-1,4,7,10-tetraoctowy, DFO - desferoksyamina , DTPA- kwas dietylenotriaminopentaoctowy. Na rysunku: chelator połączony wiązaniem peptydowym z białkiem (-CONH-Peptide) [1,4]. Zmienione.
Radioizotop Indu-111Ind należący do trzynastej grupy układu okresowego pierwiastków. Jedynym stabilnym stopniem utlenienia indu w roztworze wodnym jest stropień plus trzeci. Ze względu na duży rozmiar atomu 111In3+ przyjmuje liczby koordynacyjne w zakresie 7 - 8. Jest to mocno kwaśny katon, który chelatowany jest przez związki takie jak kwas dietylenotriaminopentaoctowy (DTPA), kwas 1,4,7-triazacyklononano-1,4,7-trioctowy (NOTA) oraz DOTA. 111ln (t1/2 = 68 h) jest najbardziej znanym radiometalem SPECT zaraz po 99mTc. Ten radioizotop rozpada sie przez wychwyt elektronu emitując fotony o energiach 173 oraz 247 keV, przez co znalazł szerokie zastosowanie w scyntygrafii gamma. 111ln nadaje się do tworzenia wraz z nim radiofarmaceutyków opartych na antyciałach monoklonalnych do radioimmunoobrazowania SPECT (immuno-SPECT). Radioizotop indu-111 produkowany jest w cyklotronie. Następnie zostaje oddzielony od materiału tarczy srebrowej lub kadmowej za pośrednictwem współstrącenia z La(OH)3 lub Fe(OH)3. Ostateczne wydzielenie 111In z zanieczyszczeń następuje przez chromatografię jonowymienną.
Mimo tego, że w handlu dostępne są pewne małe kompleksy 111In do SPECT, to radiometal ten przede wszystkim stosowany jest do opracowywania koniugatów z przeciwciałami monoklonalnymi do obrazowania SPECT. Najczęstszym stosowanym sposobem wiązania 111In do przeciwciała jest wykorzystanie chelatorów dwufunkcyjnych. Najbardziej opłacalnym chelatorem dla 111ln są pochodne DTPA.
W przeszłości większość badań immuno-SPECT przeprowadzano stosując jako źródło promieniotwórcze jod-131 (radionuklid niemetaliczny). Badania porównawcze pomiędzy 131I i 111ln wykazały, że ind dociera do nowotworów poprzez krew o wiele szybciej. Poza tym posiada dłuższy czas retencji radioaktywności w guzie, co przekłada się na jaśniejsze obrazy. Istnieją jednak znaczne niedogodności związane z użyciem 111In. Główną wadą jest wysoki niespecyficzny wychwyt radiometal w wątrobie, nerkach i śledzionie pacjenta. Wyeliminowanie tego problemu jest obecnie głównym nurtu badań radiochemicznych dla tego radioizotopu.
Chcąc zmniejszyć niespecyficzność wiązania radioimmunofarmaceutyków opartych na indzie-111, przeprowadzono modyfikacje chelatorów indu, takie jak wprowadzenie łącznika pomiędzy kompleksem, a nośnikiem. Obecnie nowe znakowane indem małe peptyd oraz przeciwciała monoklonalne wykazują obiecujące wyniki (mniejsze pobieranie przez nerki) w obrazowaniu SPECT. Stabilności w tkankach oraz biodystrybucja (wychwyt w guzie, wątrobie, nerkach), są porównywalne przy zastosowaniu DOTA, NOTA oraz DTPA (Rys. 6).
Ostatnio, trzy przeciwciała znakowane indem-111 (ProstaScint, OncoScint i MyoScint) zostały zatwierdzone do stosowania u ludzi. Wszystkie trzy zatwierdzone radiofarmaceutyki wykorzystują do kompleksowania indu-111 dwufunkcyjnego chelatora DTPA. Przeciwciało o nazwie handlowej ProstaScint skierowane jest na specyficzny błonowy antygen prostaty (PMSA), którego nadekspresję stwierdzono w komórkach gruczolakoraka prostaty. OncoScint lokalizuje lub wiąże się specyficznie z glikoproteinami błonowymi komórek nowotworowych TAG-72 gruczolakoraka jelita grubego i jajnika. MyoScint wiąże się z komórkami mięśnia sercowego, co pozwala obrazować jego zawał.
Technika SPECT cieszy się w dzisiejszych czasach duża popularnością w zastosowaniach diagnostyki obrazowej. Opracowywane są nowe bardziej specyficzne nośniki radionuklidów SPECT oraz nowe czujniki detektorów. Pomimo tego, że skanery PET oferują znacznie lepszą rozdzielczość obrazu to i tak skanery SPECT są stosunkowo mniej kosztowne, ze względu na dostępność opłacalnych długożyjących izotopów.
Autor: Karolina Wójciuk
Literatura
1. Eberle, A.N., Mild, G., Froidevaux, S., 2004. Receptor-Mediated Tumor Targeting with Radiopeptides. Part 1. General Concepts and Methods: Applications to Somatostatin Receptor-Expressing Tumors. J. Recept. Signal Transduct. Res. 24(4), 319-455.
2. http://withfriendship.com/user/sathvi/single-photon-emission-computed-tomography.php
3. Alexiou ,G.A., Tsiouris, S., Kyritsis, A.P., Fotakopoulos, G., Goussia, A., Voulgaris, S., Fotopoulos, A.D., 2010. The value of 99mTc-tetrofosmin brain SPECT in predicting survival in patients with glioblastoma multiforme. J. Nucl. Med. 51(12), 1923-6.
4. Bhattacharyya, S., Dixit, M., 2011. Metallic radionuclides in the development of diagnostic and therapeutic radiopharmaceuticals. Dalton Trans. 40(23), 6112-28.
5. Madsen, M.T., 2007. Recent advances in SPECT imaging. J. Nucl. Med. 48(4), 661-673.



Recenzje