Zdjęcie:
http://naturalia.blox.pl/2012/01/Zbawienne-dzialanie-kwasu-hialuronowego.htmlWażną właściwością kwasu hialuronowego są jego naturalne właściwości żelujące. Jedna cząsteczka kwasu wiąże aż 250 cząsteczek wody, ponadto z racji tego, że kwas ten występuje w takiej samej postaci we wszystkich organizmach, otrzymywanie go jest bardzo łatwe. Kwas hialuronowy występuje w gałce ocznej w ciele szklistym, a także w płynie łzowym i cieczy wodnistej. W okulistyce stosowane są jego sole, określane mianem hialuronianów.
Hialuronian stosowany jest także w chirurgicznym leczeniu zaćmy, utrzymuje prawidłową głębokość przedniej komory oka oraz chroni rogówkę przed wysychaniem. W chirurgii rogówki tj. w przeszczepach, hialuronian tworzy wyściółkę dla nowej rogówki,dzięki czemu pozwala uniknąć formowania się zrostów, a także umożliwia skuteczniejsze zamknięcie się rany. Ponadto, wykorzystuje się go w leczeniu urazów oka, gdzie pomaga w przywróceniu poprzedniego ciśnienia oraz zapobiega zrostom [7].
ChondroitynaJest glikozaminoglikanem, którego jednostką strukturalną jest dwucukier chondrozyna. Chondrozyna zbudowana jest z kwasu D-glukuronowego, który połączony jest glikozydowo z N-acetylogalaktozaminą. Łańcuch chondroityny (tj. 100-200 dwucukrów) powstaje w wyniku liniowej polimeryzacji chondrozyny wiązaniami glikozydowymi. Co ciekawe, chondroityna wystepuje jedynie w rogówce oka (nie stwierdzono jej obecności w innych tkankach) [9].
Siarczan dermatanuSiarczan dermatanu zaliczany jest do wyjątkowych glikanów wśród polisacharydów siarkowych, a to ze względu na fakt, że zawiera rzadko spotykany izomer kwasu glukoronowego tj. kwas L-iduronowy. Ponadto, związek ten różni się od pozostałych siarczanów chondroityny tym, że posiada całkowitą odporność na działalność hialuronidazy rozkładającej oba pozostałe siarczany chondroityny [9].
Siarczan keratanuSiarczan keratanu, dawniej znany jako keratosiarczan, wyróżnia się brakiem w cząsteczce kwasu uronowego. W jego strukturze wyróżnia się równe ilości D-galaktozy a także N-acetylo-6-O-sulfo-D-glukozaminy, które połączone są wiązaniami glikozydowymi. Siarczan keratanu występuje we wszystkich tkankach zwierzęcych , ponadto obok siarczanów chondroityny jest podstawowym składnikiem proteoglikanów. Największe ilości siarczanu keratanu odnotowuje się w rogówce oka, gdzie stanowi on ok. 50% całkowitej ilości GAG- to właśnie taki skład zapewnia rogówce przeźroczystość [9].
Zdjęcie: wzór heparyny, [8].
Heparyna, jest naturalnym antykoagulantem, jej działanie polega na zapobieganiu powstawania skrzepów. Substancja ta wytwarzana jest przez komórki tuczne, zaś z chemicznego punktu widzenia jest mieszaniną ujemnie naładowanych makrocząsteczek o różnej masie.
Działanie heparyny opiera się na wzmacnianiu działania białkowego czynnika krzepnięcia tj. antytrombiny, dzięki czemu może ona przerywać kaskadę krzepnięcia na każdym etapie, realizowanym w osoczu (heparyna wiąże również wapń - kofaktor wielu białek uczestniczących w krzepnięciu osoczowym). Tak więc, wykazuje ona silne działanie in vivo i ex vivo po podaniu dożylnym (działanie natychmiastowe) lub podskórnym [8], [11].
Dzięki kompleksowemu i prawie natychmiastowemu działaniu po dożylnym podaniu, heparyna stosowana jest do leczenia wielu poważnych chorób i dolegliwości, a także w profilaktyce stanów chorobowych. Tak więc stosuje się ją przy wszystkich zaburzeniach procesów krzepnięcia i przy krwawieniach związanych z powstawaniem skrzepów wewnątrz naczyń krwionośnych. Ponadto, dzięki swojemu działaniu ex vivo (czyli w krwi poza układem krwionośnym), heparyna jest stosowana w zabiegach wymagających zastosowania tzw. krążenia pozaustrojowego [8], [11].
Ilościowe oznaczanie heksosamin (zmodyfikowana metoda Elsona-Morgana) [2].
Heksozaminy są związkami, które w podwyższonej temperaturze oraz w środowisku zasadowym ulegaja degradacji. Z kolei, w obecności acetyloacetonu powstają chromogeny (głównie 2-metylopirol), które z kolei łatwiej ulegają kondensacji w środowisku kwasowym z aldehydem p-dimetyloaminobenzoezowym (tzw. ADAB), w wyniku czego powstaje barwny kompleks. Maksymalna absorpcja tego kompleksu przypada przy λ= 530 nm [2].
Wykonanie:Do 2 ml roztworów badanych i wzorcowych (tj. roztwór glukozaminy zawierający 200 µg D-glukozaminy w 1 ml wody 3xdestylowanej), należy dodać 0,7 ml zasadowego roztworu acetyloacetonu (przed dodaniem roztwór acetonu rozpuścić w 50 ml 0,8M roztworu Na2CO3). Probówki nalezy zamknąć szczelnie korkami z chłodniczkami zwrotnymi, po czym wstawić do wrzącej łaźni wodnej na 15 minut. Po upływie czasu inkubacji, należy dodać do próbek 4 ml etanolowego odczynnika ADAB (tj. podstawowy roztwór aldehydu p-dimetyloaminobenzoesowego: 4 g rozpuścić w 300 ml stężonego roztworu HCl cz.d.a).
Całość dobrze wymieszać , zamknąć korkiem (najlepiej z chłodnicą zwrotną) i wstawić do łaźni wodnej o temp. 75C na 30 minut. W czasie inkubacji wytwarza się trwały chromogen . Po czasie inkubacji, próbki należy ochłodzić do temperatury pokojowej i oznaczyć w nich absorbancję przy λ = 530 nm. W sposób analogiczny postąpić z próbami wzorcowymi o stężeniu 50, 100, 200 µg/ml. Z wykreślonej krzywej kalibracyjnej odczytać stężenie badanych heksozamin (próba badana) [2].
Ilościowe oznaczanie N-acetylowanej heksozaminy (J.Reissig i wsp., 1995)
Podstawą reakcji barwnej w tej metodzie jest kondensacja produktów degradacji acetylowanych heksozamin z aldehydem p-dimetyloaminobenzoesowym (ADAB). W wyniku reakcji powstaje barwny kompleks z maksymalną absorpcją przy λ= 530 nm.
Wykonanie:Do 2 probówek należy odmierzyć po 0,5 ml próby badanej, równolegle należy sporzdzić serię roztworów wzorcowych zawierających 25, 50, 100 ug N-acetyloglukozaminy. .Próba kontrolna powinna zawierać 0,5 ml wody (3x destylowanej). Do wszystkich probówek dodać 0,1 ml czteroboranu potasu (tj. 0,8M roztwór czteroboranu potasu o pH= 9.1), a następnie umieścić je we wrzącej łaźni wodnej na dokładnie 3 minuty, co ma bardzo istotne znaczenie w tym doświadczeniu, ponieważ każde przedłużenie czasu inkubacji powoduje spadek intensywności barwy [1].
Po upływie inkubacji, próbki należy natychmiast schłodzić w wodzie z lodem, a dalej dodać do nic 3 ml roboczego roztworu ADAB (tj. rozpuścić 10 g ADAB cz.d.a. w 100 ml lodowatego kwasu octowego (CH3COOH) zawierającego 12,5% HCl- roztwór podstawowy, z kolei roztwór roboczy ADAB otrzymuje się przez zmieszanie 1 objętości roztworu podstawowego z 9 objętościami lodowatego kwasu octowego- wykonuje się to bezpośrednio przed użyciem) [1].
Następnie, probówki zamknąć korkami i wstawić do łaźni wodnej o temperaturze 38C na 20 minut. W tym czasie następuje rozwój chromogenu, którego absorbancję należy oznaczyć przy λ=545 nm wobec próby kontrolnej [1].
Autor: Lidia KoperwasLiteratura:
[1]. Reissig J.L., Strominger J.L., Leloir L., 1995. A modified colorimetric method for the estimation of N-acetylamino sugars. J. Biol. Chem., 217: 959-962.
[2]. Belcher B., Nutten A.J., Sambrook C.M., 1954. The determination of glucosamine. The Analyst, 79: 201-205.
[3]. Daroszewski J., Rybka J., Gamian A., 2006. Glycosaminoglycans in the pathogenesis and diagnostics of Graves’s ophthalmopathy. Postepy Hig Med Dosw. (online), 2006; 60: 370-378
[4]. Głowacki A., Koźma E. M., Olczyk K., Kucharz E.J.: Glikozoaminoglikany - struktura i funkcja. Post. Biochem.,1995;41,139-148 [PubMed]
[5]. Koźma E.M., Głowacki A., Olczyk K., Jaźwiec M.: Proteoglikany - struktura i funkcja. Post. Biochem.,1997;43,158-172 [PubMed]
[6]. Żak I, Węglowodany , http://biochigen.slam.katowice.pl/podrecznik/10.pdf]
[7]. Dr n med. Krzemińska S. Kwas hialuronowy w medycynie, Farmakoterapia. http://www.wydawnictwoapteka.pl/files/UserFiles/file/SF_07-08_2010/8-10%20kwas%20hialuronowy.pdf
[8]. http://www.neutralizacja-heparyny.pl/cele/heparyna
[9]. Kłyszejko-Stefanowicz L, 2003. Ćwiczenia z biochemii. Wydawnictwo Naukowe PWN, 2003, s. 283-288.
[10]. Stryer L., 2003. Biochemi, Wydanie czwarte, s. 506-507. PWN 2003.
[11]. Liu J., Thorp S. C.: Cell surface heparan sulfate and its roles in assisting viral infections. Med. Res. Rev. 2002, (22, 1-25)


 Glikozaminoglikany są cukrami powszechnie wystęującymi w organizmach roślinnych i zwierzęcy. Ze względu na swoje wielorakie właściwości znalazły szerokie zstosowanie, m.in w medycynie. Ponadto pełnią bardzo ważne funkcje biologiczne i fizjologiczne, co jeszcze bardziej podkreśla fakt, że są one niezwykłymi cząsteczkami.
Glikozaminoglikany są cukrami powszechnie wystęującymi w organizmach roślinnych i zwierzęcy. Ze względu na swoje wielorakie właściwości znalazły szerokie zstosowanie, m.in w medycynie. Ponadto pełnią bardzo ważne funkcje biologiczne i fizjologiczne, co jeszcze bardziej podkreśla fakt, że są one niezwykłymi cząsteczkami. 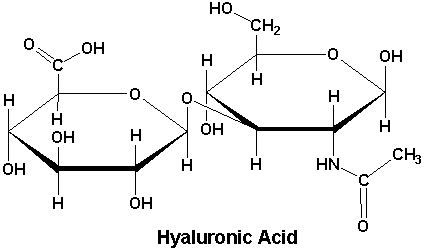
Recenzje