

|
Zamknij X
|
Z roku na rok coraz bardziej wzrasta zainteresowanie pierwiastkiem ołowiu (Pb). Ołów jest pierwiastkeim szeroko rozpowszechnionym w przyrodzie. Znajdziemy go w glebie, wodzie, żywności i w powietrzu. Duże ilości ołowiu dostają się do środowika wskutek działalności człowieka, ponieważ ołów metaliczny i jego tlenki znalazły szerokie zastosowanie w przemyśle. Wykorzystuje się go przy produkcji akumulatorów, baterii ołowiowych czy kabli i drutów [1]. Z kolei, kadm jest metalem występującym w rudach cynkowych i ołowiowych. W skutek wietrzenia skał pierwiastek ten uwalniany jest do środowiska. Podobnie jak ołów- kadm dostaje się do środowiska głównie wskutek działalności człowieka [1], [8].
Źródłem ołowiu kumulującego się w organizmie człowieka jest woda pitna oraz dym papierosowy. Jednak do organizmu pierwistek ten dostaje się głównie drogą pokarmową. Związki organiczne, a głównie alkilowe absorbowane są łatwo również przez drogi oddechowe i skórę. W produktach spożywczych ołów występuje zazwyczaj w formie nieorganicznej jako: sole, tlenki i siarczki. Po wchłonięciu z przewodu pokarmowego, żyłą wrotną ołów transportowany jest do wątroby i ogólnego krążenia, gdzie we krwi wiązany jest przez błony erytrocytów. W zależności od ukrwienia i powinowactwa pierwiastek ten kumulowany jest w różnych tkankach. Na początku odkłada się w wątrobie, nerkach, sercu i mózgu, a później w skórze, mięśniach czy tkance kostnej, z której jest bardzo wolno uwalniany. Ołów w kościach wykazuje zdolność do zastępowania jonów wapnia, a w tkance tej skumulowane jest 95% ołowiu zawartego w organizmie [1].
Przy odpowiedniej diecie około 75% spożywanego ołowiu zostaje wydalone z moczem, 16% z kałem, a pozostała ilość np. przez paznokcie czy włosy. Wzrost nagromadzenia tego pierwiastka w organizmu zależy od narażenia oraz wieku na skutek kumulacji. Kumulacja ołowiu w organizmie zaczyna się już w życiu płodowym, ze względu na łatwość przenikania przez łożysko. Stężenie ołowiu we krwi nie powinno być większe niż 40 µg /100 cm3, zaś w moczu nie większe niż 80 µg/dm3. Normy przekroczone powyżej 120 µg/100 cm3 we krwi oraz 250 µg/100 cm3 w moczu wskazują na zatrucie tym metalem i automatycznie pojawia się wiele zaburzeń zdrowotnych z tym związanych [1].
Przeprowadzone badania wskazują, że metale ciężkie posiadają zdolność do pośredniego indukowania stresu oksydacyjnego. U podłoża patofizjologicznego niektórych oddziaływań toksycznych ołowiu, kadmu czy arsenu leży nasilanie produkcji wolnych rodników, bądź też osłabianie mechanizmów obronnych. Gurer H., i wsp. (2000) do zasadniczych mechanizmów indukowania stresu oksydacyjnego przez ołów zaliczają:
1) bezpośredni wpływ ołowiu na błony komórkowe (zwłaszcza błony czerwonych krwinek),
2) interakcje między ołowiem i hemoglobiną,
3) tworzenie reaktywnych form tlenu (reakcja indukowana przez kwas d-aminolewulinowy-ALA),
4) wpływ ołowiu na antyoksydacyjne układy obronne [5].
Jak wykazano, ołów wywiera toksyczny wpływ na strukturę i funkcję błon komórkowych (szczególnie na błony erytrocytów), a to dlatego, że krwinki czerwone cechują się wysokim powinowactwem do tego metalu. Wiążą one 99% Pb zawartego w krążeniu, a także wykazują większą wrażliwością na uszkodzenia oksydacyjne w porównaniu do pozostałych komórek [5].
Kadm
Głównym źródłem kadmu u osób nienarażonych są produkty spożywcze oraz woda pitna. Ponadto, duże ilości tego pierwiastka występują w nawozach fosforowych. Kadm jest szybko absorbowany z gleby przez system korzeniowy roślin, dlatego też to właśnie warzywa, zboża i owoce są produktami, które dostarczają największe jego ilości. U ludzi wchłanianie kadmu odbywa się głównie w jelicie cienkim, a poziom wchłaniania wynosi ok. 5% ilości zawartej w diecie. Ponadd 70% całkowitej ilości wchłoniętego kadmu wiązana jest we krwi przez krwinki czerwone. W osoczu kadm łączy się z wysokocząsteczkowymi białkami, które to odkładają się w wątrobie. Następnie, związek uwalniany jest z tych połączeń i wiąże się z innym białkiem (tzw. metalotioneiną- MT).
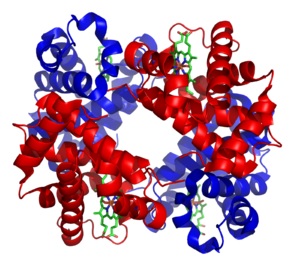
Zdjęcie:struktura białka- metalotioneina (MT), http://www.lookfordiagnosis.com/mesh_info.php?term=Metalotione%C3%ADna&>
Metalotioneina jest niskocząsteczkowym białkiem (6-7 kDa), które po raz pierwszy zostało zidentyfikowane w korze nerki u koni (1957 r.). Wtedy to nazwano ją białkiem wiążącym kadm. Jak wykazały późniejsze badania metalotioneina odgrywa bardzo ważną rolę w metabolizmie kadmu [1], [6]. Tworzone kompleksy kadmu i metalotioneiny uwalniane są do osocza, gdzie następnie w wyniku przesączania kłębuszkowego wydalane są z moczem. U osób dorosłych zawartość kadmu w organizmie wynosi od 5 do 40 mg, a 80% tego metalu ulega magazynowaniu w wątrobie oraz w nerkach. Mniejsze ilości kadmu gromadzone są w trzustce i jelitach. Co ciekawe, kadm związany z metalotioneiną nie wykazuje właściwości toksycznych, zaś wolne jony tego metalu po związaniu z innymi pierwiastkami (np. cynkiem, miedzią, żelazem, magnezem) utrudniają ich metabolizm w organizmie i prowadzą do wielu zmian morfologicznych i czynnościowych w określonych narządach [1].
Fotokolorymetryczne oznaczanie ołowiu [1].
Zasada metody opiera się na oznaczeniu z wykorzystaniem fotokolorymetrii. Reakcja polega na utworzeniu kompleksu ołowiu z ditizonem w wyniku niespecyficznej reakcji, gdzie dodatkowo należy wyeliminować inne pierwiastki, które również mogą tworzyć barwne kompleksy z ditizonem. W trakcie oznaczenia konieczne jest więc dodawanie tzw. substancji blokujących, które łącząc się z jonami przeszkadzającymi tworzą bardziej trwałe połączenia niż kompleksy z ditizonem (cyjanki, rodanki, tiosiarczany).
W celu utrzymania w roztworze jonów wapniowych, magnezowych i fosforowych, które mogłyby się wytrącać w środowisku alkalicznym, do roztworu dodaje się amoniakalny roztwór cytrynianu amonowego, który dodatkowo spełnia rolę buforu.
Jako materiał do badań wykorzystuje się soki i napoje owocowe, w których ołów występuje w postaci rozpuszczalnych soli. Dzięki temu też, możliwe jest pominięcie etapu mineralizacji próbki [1].
Wykonanie:
Z jednorodnej próbki laboratoryjnej soku należy pobrać 10 cm3 do kolbki stożkowej, następnie dodać 0,5 cm3 stężonego kwasu solnego (HCl). Próbkę ogzrewać do momentu zagotowania, następnie ochłodzić i przenieść ilościowo przy użyciu wody redestylowanej do cylindra szklanego (z doszlifowanym korkiem). Do próbki dodać 10 cm3 roztworu cytrynianu amonu, a następnie zalkalizować pzrez dodanie kilku kroplki stężonego roztworu amoniaku do pH=9 (przy kontroli phmetrem). W kolejnym etapie, do próbki dodać 1 cm3 chlorowodorku hydroksyloaminy, 5 cm3 cyjanku potasu oraz z biurety 10 cm3 chloroformowego roztworu ditizonu. Zawartość cylindra dokładnie wymieszać przez ok. 1,5 min. Gdy dojdzie do rozdzielenia się faz, dolną warstwę chloroformową należy ostrożnie pobrać do suchej probówki, po czym zmierzyć absorbancję przy długości fali równej λ= 510 nm (wobec chloroformu) [1].
Jednocześnie przygotować ślepą próbę odczynnikową, gdzie zamiast 10 cm3 próbki soku należy pobrać identyczną objętość wody redestylowanej oraz ślepą próbę soku, używając do ekstrakcji czystego chloroformu zamiast ditizonu.
Uwaga: po zakończeniu doświadczenia, zawartośc wszystkich cylindrów należy zlać do naczynia zawierającego roztwór KMnO4 in substantia, dzięki czemu nastąpi anaktywacja cyjanku potasu (silna trucizna!).
Na podstawie otrzymanych wyników oblicza się wartości absorbancji (Ax), które odpowiadają zawartości ołowiu w próbce badanej (soku):
Ax= As – (AO1 + AO2)
gdzie:
As - wartość absorbancji badanej próby
AO1 – wartość absorbancji ślepej próby odczynnikowej
AO2 – wartość absorbancji ślepej próby z soku.
Na podstawie wykresu krzywej kalibracyjnej należy odczytać ilość ołowiu odpowiadającą wartości absorbancji (Ax) oraz obliczyć zawartość ołowiu w badanej próbce soku w mg/dm3 (porównać z dopuszczalnymi normami) [1].
Oznaczanie ołowiu w nawozach- metoda woltamperometrii pulsowej różnicowej (wg Koffmann K., i wsp., 2012)
Aktualnie stosowanie nawozów fosforowych w rolnictwie ulega ciągłemu zmiejszeniu, co wiąże się ze wzrostem cen jednostkowych składników odżywczych. To, z kolei ma natychmiastowe odbicie w cenach. Zawarty w nawozach fosfor powoduje nie tylko wzrost, ale i stabilizację produkcji roślinnej. Tak więc, względy ekonomiczne przyczyniły się do poszukiwania tańszych rozwiązań dla nawożenia roślin. Zawartość makro- i mikroelementów (np. ołowiu) determinuje przydatnośc określonego preparatu do celów nawozowych, a określenie stężenia metali ciężkich w danym nawozie jest kluczowe jeśli chodzi o eklologiczne i zdrowotne aspekty wykorzystywania nawozów fosforowych [2].
Materiał do badań
Materiał do badań w doświadczeniu przeprowadzonym przez Hoffmann K. i wsp., (2012) stanowiły próbki nawozu z częściowo rozłożonym fosforytem – nawozy typu PAPR (partially acidulated phosphate rock). Próbki przygotowano w laboratorium, roztwarzając fosforyty z niestechiometryczną ilością kwasu siarkowego.
Metoda woltamperometrii pulsowej różnicowej polega na przeprowadzeniu związków ołowiu znajdujących się w badanej próbce nawozu do roztworu za pomocą kwasu nadchlorowego. Następnie, metoda polega na uzyskaniu piku metalu metodą woltamperometryczną [2].
a)Przygotowanie próbek nawozów
Odważono około 3 g badanego nawozu, a następnie dodano 10 cm3 kwasu nadchlorowego. Próbkę ogrzewano do wrzenia, do momentu rozjaśnienia się koloru roztworu. Następnie, do próbki dodano 5 cm3 wody destylowanej, ponownie ogrzewano do wrzenia, po czym próbkę ochłodzono. Ochłodzoną zawartość przeniesiono ilościowo do kolby pomiarowej o pojemności 100 cm3 i całość uzupełniono za pomocą wody destylowanej. Przygotowany w ten sposób roztwór dokładnie wymieszano i przesączono na sączku. Z przesączu pobierano próbki do dalszej analizy [2].
b)Oznaczenie zawartości ołowiu
Do kolb pomiarowych o pojemności 50 cm3 wprowadzono 25 cm3 elektrolitu podstawowego (tj.: chlorek sodu i podfosforyn sodowy), 1 cm3 0,1% roztworu żelatyny (w celu minimalizacji szumów), 4,6,8 lub 10 cm3 przygotowanego roztworu próbki. Stężenie ołowiu w próbkach oznaczano z wykorzystaniem elektrochemicznego urządzenia Metrohm Autolab. Piki ołowiu rejestrowano w zakresie potencjałów od -0,2 V do -0,7V [2].
Miareczkowanie konduktometryczne do ilościowego oznaczania ilości ołowiu w próbce
Miareczkowanie jest metodą określania nieznanego stężenia roztworu (analitu) w reakcji z reagentem o znanym stężeniu (titrantem). Miareczkowanie konduktometryczne oparte jest na pomiarze przewodnictwa elektrolitycznego. Wartość przewodnictwa ulega zmianie wraz ze zmianą stężenia jonów zawartych w roztworze [3].
Ilościowe oznaczanie ołowiu w próbce z wykorzystaniem miareczkowania oparte jest na reakcji strącania:
Pb(NO3)2 + Na2SO4 → PbSO4 + 2 NaNO3
Wykonanie:
Próbkę, która zostanie poddana oznaczeniu należy ilościowo przenieść do kolby miarowej o pojemności 100 ml, po czym uzupełnić ją do kreski wodą destylowaną. Z przygotowanej próby pobrać 20 ml do naczynia konduktometrycznego o poj. 250 ml. W naczyniu umieścić mieszadełko magnetyczne oraz oczyszczoną i wysuszoną elektrodę. Następnie, do próbki dodać 25 ml acetonu i 155 ml wody destylowanej (w celu całkowitego zanurzenia czujnika w roztworze). Z biurety dodawać po 1 ml 1 M roztworu Na2SO4 – dokładnie mieszając po dodaniu każdej porcji przez 2 minuty i mierząc przewodnictwo właściwe.
Na podstawie uzyskanych pomiarów (ujmując również liczbę ml roztworu Na2SO4 i wartości odpowiadającego jej przewodnictwa) należy wykreślić krzywą miareczkowania konduktometrycznego w układzie G=f (Na2SO4) oraz obliczyć stężenie ołowiu [mg Pb2+ /litr] [4].
Oznaczanie ołowiu i kadmu w produktach spożywczych [1]
Ilościowe oznaczanie ołowiu i kadmu polega na przeprowadzeniu mineralizacji próbek na mokro, a następnie oznaczeniu w mineralizacie pierwiastków wykorzystując w tym celu np. atomową spektrofotometrię absorpcyjną lub metodę fotokolorymetryczną.
Przygotowanie odczynników i szkła do wykonania oznaczenia
Z racji tego, że ołów wyystępuje w produktach spożywczych w ilościach śladowych, a także zanieczyszcza szkło i odczynniki, wymusza specjalne oczyszczanie wszystkich używanych do oznaczenia odczynników i sprzętu szklanego w sposób podany w polskiej normie (PN-59/A-04011). Używany do oznaczenia amoniak i chloroform poddaje się destylacji, a inne odczynniki wytrząsa się z chloroformowym roztworem ditizonu (do momentu, aż przestanie on zmieniać zabarwienie). Szkło należy dokładnie umyć mieszaniną chromową, stężonym HNO3, wodą destylowana i redestylowaną, a następnie wytrawić jeszcze kilkakrotnie 0,03 % roztworem ditizonu w chloroformie. Na wszystkich etapach przeprowadzanego oznaczenia należy zachowywać szczególną czystość, a do doświadczenia używać tylko wody redestylowanej [1].
Oznaczanie ołowiu i kadmu metodą absorpcyjnej atomowej spektrofotometrii płomieniowej [1].
Mineralizacja próbki na mokro:
W moździerzu rozetrzeć na jednolitą masę niewielką ilość próbki badanej (np. wątroba wieprzowa, wołowa, drobiowa, nerki). Z dokładnością do czterech miejsc po przecinku do naczyń, w których będzie przeprowadzana mineralizacja należy odważyć po 0,5 – 1 g próbki, następnie dodać 7 ml stężonego kwasu azotowego (próbki pozostawić na 5 minut w odkrytym naczyniu pod wyciągiem). Następnie, próbki wstawić do mineralizatora (piec mikrofalowy). Mineralizację prowadzić w następujących warunkach:
- temperatura mineralizacji: 210 °C
- czas mineralizacji : 5 minut
- ciśnienie mineralizacji: 200 PSI
- użyta moc (w zależności od ilości prób poddawanych mineralizacji): 300 -1200 W [1].
Po skończonej mineralizacji (gdy ciśnienie we wnętrzu naczyń obiży się do 60 PSI, należy ostrożnie odkręcić zawór w celu odparowania tlenków azotu, po czym pozostawić próbkę do wystygnięcia. Po wystygnięciu mineralizat przenieść ilościowo do probówki wykalibrowanej na 10 cm3 [1].
Oznaczanie ołowiu i kadmu metodą atomowej spektrofotometrii absorpcyjnej
Metoda polega na pomiarze absorpcji promieniowania lampy katodowej przez wolne atomy pierwiastka znajdujące się w roztworze próbki, która wprowadzana jest do płomienia w formie rozpylonej [1].
Wykonanie:
Po włączeniu aparatu (odpowiednim ustawieniu i wygrzaniu lampy ołowiowej, lampy kadmowej i palnika) ustawia się wszystkie niezbędne parametry pomiaru dla badanego pierwiastka, a następnie zeruje się aparat. Po wyzerowaniu, gdy sygnał absorbancji jest stały należy przystąpić do właściwej analizy. Jako pierwszy etap oznaczenia należy wykreślić krzywą kalibracyjną dla ołowiu, do której będą odnoszone wyniki analizy. W tym celu przygotowuje się szereg roztworów wzorcowych o znanych stężeniach: 0,05 mg ołowiu na 1 dm3, 0,1 mg, 0,2 oraz 0,5 mg ołowiu na 1 dm3. Po ustaleniu krzywej należy zmierzyć stężenie ołowiu w próbach badanych. Analogiczne oznaczenie wykonuje się przy oznaczeniu kadmu.
Na podstawie otrzymanych wartości oblicza się miligramy badanego pierwiastka na kilogram produktu, a dalej porównuje się z aktualnie dopuszczalnymi poziomami zanieczyszczeń produktów spożywczych tymi pierwiastkami [1].
Ołów z dymu papierosowego a ciąża
W dymie tytoniowym występuje szereg metali ciężkich, w tym m.in. ołów, który w układzie oddechowym palacza wykazuje retencję na poziomie ok. 84%, co z kolei powoduje, że dym tytoniowy jest ważnym źródłem ołowiu w organizmie. Według danych przedstawionych przez WHO (World Health Organisation) w jednym wypalonym papierosie znajduje się od 17 do 980 ng ołowiu. Dym tytoniowy, a głównie zawarty w nim ołów jest szczególnie niebezpieczny dla kobiet w ciąży. Liczne badania potwierdziły, że kumulacja Pb zaczyna się już w życiu płodowym. Brak bariery łożyskowej dla jego transportu oraz nasilone uwalnianie ołowiu z kości matki prowadzi na zwiększone narażenie płodu na jego toksyczne działanie. Co więcej, zagrożenie dla płodu stwierdzono również u kobiet, które rzuciły palenie w czasie ciąży. Wiąże się to z mobilizacją ołowiu z kości matki. Wzrastający poziom Pb podczas ciąży może przyczynić się do wystąpienia przedwczesnego porodu czy samoistnych poronień. Badania dowiodły, że prenatalna ekspozycjna nawet na niskie dawki ołowiu może objawiać się niską masą urodzeniową, wystąpieniem wad rozwojowych czy zaburzeń rozwoju umysłowego i psychoruchowego [7].
Chełchowska M. i wsp., (2012) przeprowadzili badania na ciężarnych kobietach podzielonych na grupę palącą tytoń oraz abstynentek tytoniowych. Badania opierały się na pomiarze kotyniny (związku powstającego na skutek rozkładu nikotyny w organizmie człowieka), w celu oceny wpływu palenia tytoniu na poziom ołowiu w osoczu i pełnej krwi kobiet ciężarnych.
Badania dowiodły, że w grupie kobiet palących znacząco wzrasta poziom ołowiu we krwi (uzależniony od czasu trwania nałogu oraz liczby wypalanych papierosów), z kolei u abstynentek wykazano tylko śladowe ilości tego pierwiastka. We wszystkich trymestrach ciąży poziom ołowiu w osoczu krwi (Chełchowska M., i wsp., 2012) był statystycznie wyższy w grupie kobiet palących, niż w grupie abstynentek tytoniowych.
Ponadto, badania przeprowadzone przez Mi-Gyung Lee i wsp.,(2005) wykazały, że palaczki mają 4,5 razy większe prawdopodobieństwo wystąpienia wyższego stężenia ołowiu we krwi, niż to występuje u kobiet niepalących [7].
Według Rozporządzenia Komisji (WE) nr 1881/2006 z dnia 19 grudnia 2006 r. ustalające najwyższe dopuszczalne poziomy niektórych zanieczyszczeń w środkach spożywczych, maksymalne poziomy zawartości zanieczyszczeń w produktach spożywczych dla dzieci w przypadku ołowiu wynoszą 0,02 mg/kg wagi świeżego produktu [9].
Autor: Lidia Koperwas
Literatura:
[1]. [1]. Augustyniak U., Brzozowska A., Czerwińska D.,Dąbrowska M., Kałuża J., Kozłowska K., Morawiec M., Pietruszka B., Wierzbicka E., 2010. Toksykologia żywności. Przewodnik do ćwiczeń pod redakcją Anny Brzozowskiej. Wydanie IV uzupełnione. Wydawnictwo SGGW, Warszawa 2010, s. 157-169.
[2]. Hoffmann K., Kasprzyszak A., Hoffmann J., Skut J., 2012. Oznaczanie ołowiu w preparatach nawozowych typu PAPR metodą woltamperometrii pulsowej różnicowej. Proceedings of ECOpole, DOI:10.2429/proc.2012.6(1)028, http://tchie.uni.opole.pl/PECO12_1/PL/HoffmannKasprzyszak_PECO12_1.pdf
[3]. http://www.vrml.k12.la.us/rpautz/documents/Chemistry/ConductometricTitration.pdf
[4]. http://biol-chem.uwb.edu.pl/zmf/cw3_elc.pdf
[5]. Chlebda E., Antonowicz-Juchniewicz J., Andrzejak R.,2004. Wpływ ekspozycji zawodowej na ołów i arsen na stężenie karotenoidów w surowicy u pracowników huty miedzi. Medycyna Pracy 2004; 55 (5): 389 — 401. http://test.imp.lodz.pl/upload/oficyna/artykuly/pdf/full/Chl3_05_04.pdf
[6]. Sakulsak N., 2012. Metallothionein: An Overview on its Metal Homeostatic Regulation in Mammals. Int. J. Morphol., 30(3):1007-1012, 2012. http://www.scielo.cl/scielo.php?pid=S0717-95022012000300039&script=sci_arttext
[7]. Chełchowska M., Jabłonka-Salach K., Ambroszkiewicz J., Maciejewski T., Gajewska J., Bulska E., Laskowska-Klita T., Leibschang J., Braciszewski J., 2012. Wpływa palenia tytoniu na poziom ołowiu we krwi kobiet ciężarnych. Medycyna Wieku Rozwojowego, 2012, XVI, 3. http://medwiekurozwoj.pl/articles/2012-3-4.pdf
[8]. SinghN.,Singh N., Swarupa Tripathy S., Soni D., Singh K.,Gupta P.K., 2013. Evaluation of purity with its uncertainty value in high purity lead stick by conventional and electro-gravimetric methods. Chemistry Central Journal 2013, 7:108. http://journal.chemistrycentral.com/content/7/1/108
[9].http://europa.eu/legislation_summaries/food_safety/contamination_environmental_factors/l21290_pl.htm
25 maja 2018 roku zacznie obowiązywać Rozporządzenie Parlamentu Europejskiego i Rady (UE) 2016/679 z dnia 27 kwietnia 2016 r (RODO). Potrzebujemy Twojej zgody na przetwarzanie Twoich danych osobowych przechowywanych w plikach cookies. Poniżej znajdziesz pełny zakres informacji na ten temat.
Zgadzam się na przechowywanie na urządzeniu, z którego korzystam tzw. plików cookies oraz na przetwarzanie moich danych osobowych pozostawianych w czasie korzystania przeze mnie ze strony internetowej Laboratoria.net w celach marketingowych, w tym na profilowanie i w celach analitycznych.
Administratorami Twoich danych będziemy my: Portal Laboratoria.net z siedzibą w Krakowie (Grupa INTS ul. Czerwone Maki 55/25 30-392 Kraków).
Chodzi o dane osobowe, które są zbierane w ramach korzystania przez Ciebie z naszych usług w tym zapisywanych w plikach cookies.
Przetwarzamy te dane w celach opisanych w polityce prywatności, między innymi aby:
dopasować treści stron i ich tematykę, w tym tematykę ukazujących się tam materiałów do Twoich zainteresowań,
dokonywać pomiarów, które pozwalają nam udoskonalać nasze usługi i sprawić, że będą maksymalnie odpowiadać Twoim potrzebom,
pokazywać Ci reklamy dopasowane do Twoich potrzeb i zainteresowań.
Zgodnie z obowiązującym prawem Twoje dane możemy przekazywać podmiotom przetwarzającym je na nasze zlecenie, np. agencjom marketingowym, podwykonawcom naszych usług oraz podmiotom uprawnionym do uzyskania danych na podstawie obowiązującego prawa np. sądom lub organom ścigania – oczywiście tylko gdy wystąpią z żądaniem w oparciu o stosowną podstawę prawną.
Masz między innymi prawo do żądania dostępu do danych, sprostowania, usunięcia lub ograniczenia ich przetwarzania. Możesz także wycofać zgodę na przetwarzanie danych osobowych, zgłosić sprzeciw oraz skorzystać z innych praw.
Każde przetwarzanie Twoich danych musi być oparte na właściwej, zgodnej z obowiązującymi przepisami, podstawie prawnej. Podstawą prawną przetwarzania Twoich danych w celu świadczenia usług, w tym dopasowywania ich do Twoich zainteresowań, analizowania ich i udoskonalania oraz zapewniania ich bezpieczeństwa jest niezbędność do wykonania umów o ich świadczenie (tymi umowami są zazwyczaj regulaminy lub podobne dokumenty dostępne w usługach, z których korzystasz). Taką podstawą prawną dla pomiarów statystycznych i marketingu własnego administratorów jest tzw. uzasadniony interes administratora. Przetwarzanie Twoich danych w celach marketingowych podmiotów trzecich będzie odbywać się na podstawie Twojej dobrowolnej zgody.
Dlatego też proszę zaznacz przycisk "zgadzam się" jeżeli zgadzasz się na przetwarzanie Twoich danych osobowych zbieranych w ramach korzystania przez ze mnie z portalu *Laboratoria.net, udostępnianych zarówno w wersji "desktop", jak i "mobile", w tym także zbieranych w tzw. plikach cookies. Wyrażenie zgody jest dobrowolne i możesz ją w dowolnym momencie wycofać.
Więcej w naszej POLITYCE PRYWATNOŚCI
Recenzje