Wprowadzenie
Termograwimetria jest to technika, w której określa się zmiany masy badanej próbki, gdzie zmiany masy są wynikiem zadanego reżimu temperaturowego. W metodzie tej mierzy się masę próbki w funkcji temperatury. ICTAC zaleca stosowanie skrótu TGA (Thermogravimetric Analysis) zamiast dotychczas proponowanego i spotykanego w literaturze – TG (symbolem Tg oznacza się temperaturę zeszklenia ang. glass transition temperature).
Termowaga
Za pomocą komory wagowej lub wagi termograwimetrycznej (termowaga) mierzy się zmianę masy danej substancji w zależności od zmian temperatur lub upływu czasu. Próbkę w naczynku (z platyny lub trójtlenku glinu) umieszcza się w piecyku, który jest połączony z termowagą. Próbkę ogrzewa się do danej temperatury, która może sięgać do 1600 °C. Ze względu na wysoką temperaturę, piec musi być chroniony przed wstrząsem termicznym. Aby temu zapobiec, stosuje się kwarc i tlenek magnezu, jako materiały ognioodporne. Pomiar danej temperatury realizuje się przy pomocy termopary, która znajduje się bezpośrednio przy naczynku próby. Do pomiaru masy stosuje się szczególnie wrażliwą wagę elektroniczną (termowagę), wystarczająco oddaloną od pieca by uniknąć efektów korozji. Termowaga jest waga o specjalnej konstrukcji. Przeznaczona jest ona do pomiarów zmiany masy próbki podczas jej ogrzewania. Może być wyposażona w piec elektryczny lub promiennik podczerwieni oraz rejestrator zmian masy próbki w zależności od czasu nagrzewania albo temperatury. W praktyce wykorzystuje się wiele konfiguracji termowagi – układy pionowe (Rys. 1 A, B) oraz układy poziome (Rys. 1 C).
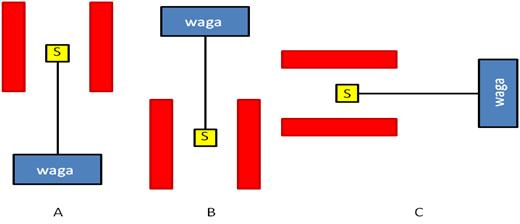
Rys. 1. Schemat klasycznych typów termowag.
Pomiary TGA rzadko przeprowadza się w warunkach próżniowych. Najczęściej ogrzewa się badaną próbkę, w atmosferze gazowej o określonym składzie, stosując program zmian temperatury z góry ustalony, niezależny od zachowania się próbki w pomiarze. Pomiary TGA prowadzi się w atmosferze utleniającej (O2, powietrze) lub w atmosferze obojętnej (N2, Ar). Nowoczesne przyrządy umożliwiają zmianę gazu w trakcie pomiaru. Gazu płuczący piec przepływa zwykle w kierunku od wagi do pieca. Reżim temperaturowy realizuje się stosując odpowiedni programator i regulator temperatury. W termograwimetrii najczęściej stosuje się stałe zmiany temperatury β = ∆T/∆t, gdzie β=const, ale β > 0. Nowoczesne termowagii pozwalają na zastosowanie programów wielosegmentowych np.: ogrzewanie + izotermia a nawet zmiany składu atmosfery gazowej). Rzadko wykonuje się pomiary termograwimetryczne polegające na ogrzewaniu próbki w sposób zależny od jej zachowania się w trakcie pomiaru. Ten typ termograwimetrii określa się angielskim terminem Controlled RateThermal Analysis (CRTA) lub Sample Controlled Thermal Analysis (SCTA). Reżim temperaturowy ustala się tak aby szybkość zmiany (zwykle ubytku) masy próbki w czasie przemiany (odwracalnej reakcji chemicznej) była stała. Ubytek masy nie może być większy, niż zaprogramowana
wartość progowa. Wynikiem pomiarów termograwimetrycznych jest krzywa termograwimetryczna (krzywa TGA). Krzywa ta jest zależnością masy próbki od czasu i/lub temperatury.
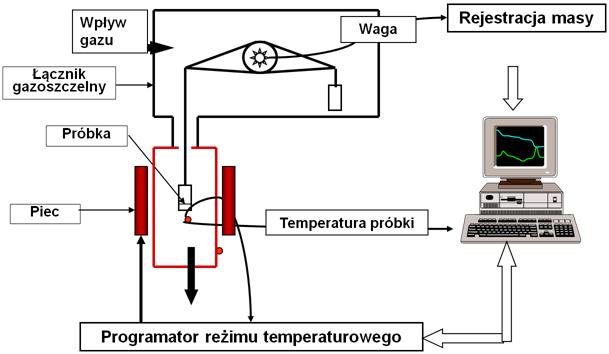
Rys.2 Schemat działania termowagii.
Przemiany próbki
Podczas pomiarów TGA badana próbka ulega przemianom fizycznym lub chemicznym. W reakcjach chemicznych mogą brać udział składniki atmosfery gazowej a nawet materiał naczyńka pomiarowego. Zmiany jakim ulegnie badana próbka zależą od wielu różnych parametrów pomiarowych takich jak: wielkość próbki analitycznej (masa, rzadziej objętość), materiał i geometria naczyńka pomiarowego, szybkość ogrzewania, rodzaj atmosfery gazowej (skład, ciśnienie, przepływ) oraz zewnętrzne pole magnetyczne. Każdy z tych parametrów wpływa na rodzaj i szybkość przemian próbki. Dzięki temu uzyskuje się dane termograwimetrycznie (skład, temperatura, kinetyka przemian itp.)
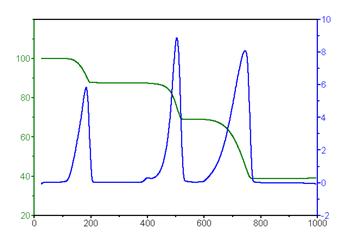
Rys. 3. Główne typy przebiegu krzywych w analizie termo grawimetrycznej. Krzywa zielona przedstawia ubytek masy [%] podczas pomiaru. Krzywa niebieska szybkość utraty masy.
Na próbkę działają siły: grawitacyjna, magnetyczna i aerodynamiczna (związana z ruchem ośrodka gazowego nad próbką). Zatem na wagę wpływa siła wypadkowa, która jest sumą wymienionych wcześniej sił:
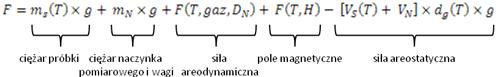
Gdzie:
F(T,H) - siła wynikająca z działania pola magnetycznego,
H – natężenie zewnętrznego pola magnetycznego,
mS – masa próbki,
mN – suma mas naczyńka pomiarowego i szalki wagi,
V – objętość,
dg – gęstość gazu,
DN – parametry geometryczne układu próbki,
g – przyspieszenie ziemskie.
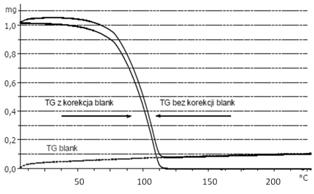
Na pomiar wykonywany w ośrodku gazowym mają wpływ siły: aerodynamiczna, aerostatyczna. Pole magnetyczne ma wpływ podczas pomiarów ze stałym zewnętrznym polem magnetycznym. Badania wykorzystujące pole magnetyczne w termograwimetrii nazywa się termomagnetometrią. W termograwimetrii bardzo ważne jest dokładne określenie masy próbki. Wyznaczenie jej polega na wektorowym odjęciu pozostałych składowych z równania (1). Aby empirycznie zastosować to odejmowanie wykonuje się pomiar blank tzw. „ślepą próbę”. Pomiar ten wykonuje się w warunkach pomiarowych dla pustego naczyńka pomiarowego. Zmiany przebiegu widma przedstawiono poniżej.
Rys.4. Krzywa termograwimetryczna po korekcji blank.
Dodatkowym utrudnieniem w pomiarze masy próbki jest tendencja przyjmowania, że temperatura próbki będzie zgodna z zadanym reżimem temperaturowym:
Tβ = To + β x t (2)
Zależność ta jest spełniona tylko dla próbki termicznie biernej, czyli takiej w której nie zachodzą przemiany fizyczne lub chemiczne egzo- endotermiczne, które mogłyby zaburzyć układ cieplny pomiędzy piecem, a próbką. Termowagi wyposażone są w czujnik temperaturowy, który mierzy temperaturę próbki. Zasadniczy wpływ na temperaturę próbki ma: temperatura pieca, właściwości cieplne próbki, naczyńko pomiarowe w którym znajduje się próbka, właściwości szalki wagi a także przewodnictwo cieplne gazu otaczającego próbkę.
Wzorcowanie termowag przeprowadza się dla substancji o znanych temperaturach przemian fizycznych w warunkach dynamicznych. W zależności od rodzaju termowagi: (1) urządzenie tylko do pomiarów termo grawimetrycznych lub termowaga połączona z dodatkowym urządzeniem (DTA, DSC). W pierwszym przypadku do wzorcowania temperaturowego używa się materiały ferromagnetyczne o znanych temperaturach punktu Curie (przemiana ferromagnetyku w paramagnetyk). Tego typu pomiary termograwimetryczne prowadzi się wówczas w zewnętrznym polu magnetycznym magnesu stałego (termomagnetometria) [4]. Zaś w drugim przypadku stosowane są substancje wzorcowe o znanych temperaturach przemian fazowych pierwszego rodzaju (topnienie, przemiany polimorficzne). Do tego typu substancji stosuje się głównie czyste metale o znanych temperaturach topnienia: cyna - Sn (231,9°C), ołów - Pb (327,5°C), cynk - Zn (419,5°C), glin - Al (660,3°C), srebro - Ag (961,8°C), złoto - Au (1064,2°C).
W pomiarze wzorcującym substancja wzorcowa pełni rolę „wewnętrznego” termometru próbki, ponieważ wskazuje jej temperaturę w punkcie przemiany. Dopiero według temperatury tej przemiany wzorcuje się czujnik temperaturowy, dzięki któremu określa się temperaturę próbki badanej. Najczęściej stosuje się kilka substancji wzorcowych (różne temperatury przemian), co pozwala wywzorcować termowagę w całym zakresie temperatur jej pracy. Stała czasowa może być obliczona wg równania (2) na podstawie wyników wzorcowania temperaturowego przeprowadzonego dla jednej wartości szybkości ogrzewania β. Częściej jednak przeprowadza się najpierw określenie zależności stałej czasowej wyprzedzenia temperaturowego od temperatury, a następnie, wykorzystuje się uzyskane wyniki do przeprowadzenia standardowego wzorcowania temperaturowe termowagi. Stałą czasową wyprzedzenia temperaturowego wyznacza się na podstawie wzoru:
τ_∆ (T_1)=〖∆T〗_m/∆β (2)
τ_∆ (T_1 ) – stała czasowa
T_m – temperatura przemiany
β – szybkość ogrzewania
Stałą czasową wyznacza się wykonując wiele pomiarów przy różnych szybkościach ogrzewania dla tej samej przemiany substancji wzorcowej. Kalibracja dla kilku substancji wzorcowych, o różnych temperaturach przemian, pozwala wyznaczyć zależność stałej czasowej wyprzedzenia temperaturowego od temperatury w całym zakresie temperatur pracy termowagi. Przy stosowaniu jednej szybkości ogrzewania, wartości bezwymiarowych współczynników. Należy pamiętać, że nie ma czysto termograwimetrycznego wzorca temperatury – substancji o punkcie zmiany masy. Dowodem poprawności wzorcowania temperaturowego termowagi, w tym właściwego uwzględnienia zależności gradientu temperatury między próbką, a czujnikiem temperaturowym od szybkości ogrzewania, jest uzyskiwanie dokładnych i niezależnych od szybkości ogrzewania wyników oznaczeń temperatur przemian fizycznych, takich jak topnienie czy przemiana ferromagnetyka w paramagnetyk.
Przy stosowaniu termograwimetrii ważna jest powtarzalność (analiza składu) lub wysoka dokładność pomiaru temperatury (analiza kinetyczna przemian chemicznych).
Analiza składu
Pomiary termograwimetryczne prowadzi się najczęściej w dynamicznej atmosferze gazowej, pod ciśnieniem atmosferycznym (rzadziej pod próżnią albo w atmosferze statycznej). Chemiczny skład atmosfery gazowej jest istotnym parametrem pomiaru, gdyż w wielu przypadkach determinuje on rodzaj chemicznych reakcji próbki, szczególnie dla związków organicznych. Reakcje te wykorzystuje się w analityce składu np. kompozycji i kompozytów polimerowych. Jakościową analizę składu układów wieloskładnikowych w termograwimetrii przeprowadza się na podstawie analizy etapów ubytku masy zinterpretowanych jako powodowane przez określone reakcje składników próbki. Analiza składu za pomocą termograwimetrii przedstawiona jest w pracach Balcerowiaka.
Analiza kinetyczna
Wielkością fizyczną zależną od stopnia konwersji substratu lub substratów reakcji (przebiegu reakcji chemicznej) jest masa. Jeżeli produktem lub substratem reakcji jest substancja lotna (w temperaturze powstawania) lub mieszanina gazów o stałym składzie, to chwilowy stopień konwersji substratu reakcji jest określony na podstawie wielkości zmiany masy badanej próbki w czasie. Zmiana masy próbki jest obserwowana w stosunku do wielkości zmiany masy odpowiadającej 100% wydajności reakcji. Dane do analizy kinetycznej omawianych większości typów reakcji chemicznych stanowią wówczas szeregi par wartości: α–t (dla T = const) albo α–T (dla b = const). Gdzie α opisane jest wzorem (3):
∝=(m_0-m_t)/ (m_0-m_f) (3)
m_0 - masa wyjściowa
m_t – masa po upływie czasu t
m_f - masa próbki po całkowitym przereagowaniu substratów

Tab.1 Przemiany chemiczne i fizyczne w termograwimetrii.
Interpretacja wyników
Przeprowadzając doświadczenia oraz interpretując otrzymane wyniki analiz TG należy pamiętać, że uzyskany w trakcie pomiarów wynik jest silnie uzależniony od warunków, panujących podczas pomiaru. Wpływ warunków pomiarów na uzyskany wynik jest bardzo istotny. Poznanie i rozumienie wpływu różnych parametrów pomiaru na uzyskiwane kształty sygnałów w TG pozwala na poprawną interpretację. Przebieg krzywych TG uzależniony jest od następujących czynników:
– aparatura (konstrukcja oraz sposobów prowadzenia eksperymentów, rodzaj, typ i klasa dokładności wykorzystanej aparatury oraz materiał, konstrukcję i masę naczyniek, w których umieszczona jest próbka, a także szybkość zmian temperatury i rodzaj substancji wzorcowej)
– forma badanej substancji (masa próbki, przewodnictwo cieplne i pojemność cieplną próbki oraz ich zależności temperaturowe)
– budową chemiczną substancji oraz reakcje jakim ulega (zmiana masy próbki – będącą wynikiem przebiegu reakcji i wydzielania produktu gazowego lub będącą efektem reakcji pomiędzy składnikiem atmosfery a próbką, dodatkowo czynnik ten zależy od rodzaj gazu tworzącego atmosferę a nawet szybkości jego przepływu; reakcji następczych i równoległych oraz od parametrów kinetycznych i wielkość efektów cieplnych dotyczących badanej próbki.
Zastosowania termo grawimetrii
Zdolność do generowania, w analizie termograwimetrycznej podstawowych danych z niemal każdej klasy materiałów doprowadziło do jej powszechnego stosowania niemal w każdej dziedzinie nauki i techniki. Główne obszary zastosowań są wymienione poniżej:
1. Stabilność termiczna: każdy typ materiału zmoże być badany w podwyższonych temperaturach. Krzywa TG może pomóc wyjaśnić mechanizmy rozkładu.
2. Badania kinetyczne: procesów chemicznych syntezy, rozpadu, jak i wymiany.
3. Charakterystyka materiałów: krzywe TG i DTG uważane są za tzw. "odcisk palca” danych substancji dlatego też mogą być użyte do identyfikacji i kontroli jakości.
4. Badania korozji: TG stanowi doskonałą metodę badania procesów utleniania
5. Symulacja procesów przemysłowych: piec termowagi może być traktowany jako mini-reaktor, z możliwością imitowania warunków panujących w niektórych typach reaktorów przemysłowych.
6. Analizy składu (omówiona powyżej)
TGA a DSC
Połączenie obu metod analizy termicznej TGA i DSC, pozwalających na badanie zmian wybranych właściwości fizycznych substancji pod wpływem zmieniającej się w określony sposób temperatury, umożliwia dokonanie oceny wybranych procesów, zachodzących w określonej substancji. Zastosowanie równocześnie obu metod analizy termicznej wykorzystywane jest m.in. do badania reakcji chemicznych i przemian fazowych zachodzących podczas ogrzewania substancji, do wyznaczania parametrów termodynamicznych i kinetycznych reakcji, a także do wyznaczania i porównywania trwałości termicznej badanych substancji.
Podsumowanie
TG mierzy ilość i szybkość zmian w wadze materiału jako funkcję temperatury albo czasu w kontrolowanej atmosferze. Używane jest ona głównie by określić skład materiałów oraz do określenia ich stabilności cieplnej przy temperaturach nawet do 1000°C. Technika charakteryzuje materiały , które poprzez spadek wagi albo jej zysk z powodu rozkładu, utlenianie i innych reakcji chemicznych.
Streszczenie
Analiza termograwimetryczna zwana także cieplną grawimetria (TGA) jest
to pomiar zmiany masy badanej próbki w stosunku do zmiany temperatury. W tym typie analizy są rejestrowane zmiany wagi, i temperatura. Powstaje
krzywa, która jest pochodną spadku masy. Może być ona interpretowana
bezpośrednio lub po dekonwolucji otrzymanego widma. Metoda ta ma swoje
zastosowanie w analizie składu, jak i analizie kinetycznej.
SkrótyCRTA/SCTA – termograwimetria ze zmiennym reżimem temperaturowym
DSC – różnicowa kalorymetria skaningowa
Tg – temperatura zeszklenia
TG – dawny skrót termograwimetrii
TGA – termograwimetria
Literatura1. ICTAC Nomenclature of Thermal Analysis. 2004. ICTAC News. 37(2): 62-70
2. Hemminger W., Wilburn F.W., Gravelle P.C., Haglund B.O., Hianes P.J., Hakvoort G., Ohlyba M., Simon J., Sarge S.M. 1998. ICTAC Nomenclature Committee Report: „Recommendation for Names and Definitions in Thermal Analysis and Calorimetry”. ICTAC News, 31(2):107-122
3. Balcerowiak W.1988. TG base line, J. Thermal Anal., 33: 211-215
4. Gallacher P.K. 1998. Thermogravimetry and Thermomagnetometry, w P.K. Gallacher (ed.serii), Handbook of Thermal Analysis and Calorimetry, M.E. Brown (ed. vol. 1): Principles and Practice, Elsevier 225-278
5. Balcerowiak, Wasilewski J., Latocha C. 1980. Thermoanalytical investigation of mixtures containing W. oxalic acid, sodium hydrogen oxalate and sodium oxalate, J. Thermal Anal. 18: 57
6. Balcerowiak W.2003. Thermal properties of rhodium (III) chloride. Rhodium content determination. J. Thermal Anal. Cal., 75: 559-565
7. Balcerowiak W., Terelak K., Trybuła S. 1995. Thermogravimetric examination of polyalcohol- formate binary systems, J. Thermal Anal., 45: 1231-1237
8. Balcerowiak W. 1997. Speciation analysis of sulfonic groups of cation exchanger using thermogravimetry, Reactive & Functional Polymers, 33: 323-327
9. Balcerowiak W. 2000. Phase analysis of high-calcium lime by TG, J. Thermal Anal. Cal. 60: 67-70
10. Balcerowiak W., Thermal properties of rhodium (III) chloride. Rhodium content determination, J. Thermal Anal. Cal., 71: 559-565
11. Małecki A. 2002 Wpływ różnych czynników na wyniki pomiarów DTA/DSC/TG. Materiały konferencyjne – III Szkoła Analizy Termicznej, s. 77–159. Zakopane 2002
opracowała: Karolina Wójciuk
wstecz
Podziel się ze znajomymi