

|
Zamknij X
|
Historia atomu
Już starożytni filozofowie greccy zadawali pytania o to z czego zbudowana jest otaczająca nas materia. Jedna z teorii, którą głosił Demokryt z Abdery, mówiła o istnieniu niepodzielnego składnika atomos. Nie była to wszakże teoria naukowa, ale rozprawą filozoficzną na temat budowy materii.
Zwolennikami teorii atomistycznej był m in. żyjący w latach 1627 - 1691 Robert Boyle oraz słynny fizyk, matematyk, astronom Izaak Newton. Wraz z rozwojem nauki, hipoteza istnienia atomu zaczynała być coraz bardziej prawdopodobna, chodź we wczesnych latach dwudziestego wieku wielu naukowców wciąż nie wierzyło w istnienie atomów.
Atom, istnieje na prawdę.
Francuski naukowiec Antoine-Laurent Lavoisier pracując nad prawem zachowania masy w chemii opisał, w swojej pracy z 1789 roku Traité Élementaire de Chimie (Elementy Chemii), pierwiastki jako niepodzielne elementy materii [1]. Cztery lata później John Dalton w pracy A New System of Chemical Philosophy głosił teorię atomizmu. Zakładał on, że materia zbudowana jest z atomów, a każdy pierwiastek składa się z atomów tego samego rodzaju (Rysunek 1).

Rysunek 1: Oznaczone przez Johna Daltona pierwiastki, zdjęcie z traktatów A New System of Chemical Philosophy.
Pierwszy model struktury atomu zaproponował angielski fizyk Joseph John Thompson w swojej pracy z 1904 roku. Badając promieniowanie katodowe odkrył on istnienie elektronu. Ostatecznie odkrycie to zaprzeczyło teorii niepodzielności atomu [2]. Model Thomhsona zakładał istnienie ujemnie naładowanych elektronów, które poruszały się w jednorodnej dodatnio naładowanej kuli, stąd nazwano go ciastkiem z rodzynkami (Rysunek 2 a)). Model ciastka z rodzynkami został obalony, gdy w 1909 Ernest Marsden i Hans Geiger pod kierunkiem Ernest Rutherforda przeprowadzili słynny eksperyment, bombardowali oni złotą folię cząstkami alfa [3]. Model Thompsona nie wyjaśniał dobrze, dlaczego część cząstek alfa przelatuje inne zaś rozpraszają się na złotej folii. W roku 1911 Ernest Rutherford zaproponował nowy model atomu. Zakładał on, że większość masy skupiona jest w dodatnim jądrze, a ujemnie naładowane elektrony krążą wokół niego. Były to założenia zbliżone współczesnemu modelowi. Niedługo później, bo w roku 1913, Niehls Bohr opublikował pracę, w której zaproponował model budowy atomu wodoru [4]. Model ten oparł się na dwóch postulatach. Po pierwsze: moment pędu elektronu przyjmuje tylko pewne wartości (nħ, ħ jest tzw. zmodyfikowaną stałą Plancka, natomiast n jest dowolną liczbą naturalną). Po drugie: elektron może przejść z jednej orbity na inną dozwoloną (Rysunek 2 b)) czemu towarzyszy wypromieniowanie (bądź zaabsorbowanie) fotonu (porcji światła) o energii równej różnicy energii tych poziomów.
a)

b)
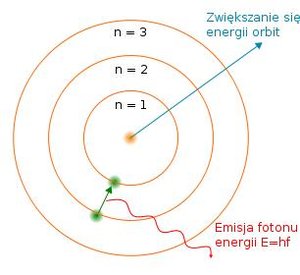
Rysunek 2: a) Model atomu Thompsona (ciastko z rodzynkami), ujemnie naładowane elektrony znajdują się wewnątrz jednorodnej dodatnio naładowanej kuli. b) Model atomu wodoru Bohra, w centralnej części znajduje się jądro (proton) wokół którego krąży elektron.
Elektron porusza się po orbitach o ściśle określonej energii (Eelektronu = nħ). Przejściu elektronu z jednej orbity na drugą towarzyszy wypromieniowanie bądź pochłonięcie energii w postaci fotonu (porcji światła) o energii równej różnicy energii tych orbit (Ewypromieniowane/pochłoniete = hf, gdzie h jest wielkością stałą w fizyce stała Plancka, a f częstotliwością wypromieniowanego światła) [5].}

Rysunek 3: Drabinka energetyczna. Elektron może znajdować się tylko w ściśle określonym stanie, który reprezentują szczebelki drabinki. Przyjmuje on więc jedynie określone wartości energii.
Atom dziś.
Model atomu wodoru zaproponowany przez Nielsa Bohra zakładał, że wokół protonu (jądra) po kołowych orbitach krąży elektron (Rysunek 2 b)). Energia jaką może przyjmować elektron jest ściśle określona. Doskonale obrazuje to zamieszczona na Rysunku 3 drabinka. Każdy ze szczebelków drabinki reprezentuje jakąś wartość energii, a sam elektron może wędrować w górę i w dół drabinki ale tylko po szczebelkach. Nie może posiadać innej energii.
Zgodnie z założeniami mechaniki klasycznej elektron poruszający się po kołowej orbicie powinien wypromieniowywać energię, a w konsekwencji spaść na jądro. Tak się jednak nie dzieje, a wytłumaczenie pojawiło się wraz z odkryciem mechaniki kwantowej.
Jądro atomowe wodoru składa się z jednego dodatnio naładowanego protonu. Atomy bardziej złożonych pierwiastków składają się nie tylko z dodatnich protonów ale i z elektrycznie obojętnych neutronów. Nukleony, bo tak nazwano cząstki budujące jądra atomowe, są dużo cięższe od elektronów, a ich masy są do siebie zbliżone. Praktycznie cała masa atomu skupiona jest więc w jego centrum. Rozmiary jądra atomowego są rzędu 10^{-15}, natomiast rozmiar całego atomu (wraz z krążącymi wokół jądra elektronami) to rząd wielkości 10^{-10} m [6]. Gdyby więc jądro atomowe miało promień 1 metra, to jego pierwszy elektron krążyłby po orbicie o promieniu około 100 km.
Dzięki mechanice kwantowej poznaliśmy właściwości atomów, które pozwoliły na dalsze odkrycia. Skonstruowano lasery, które emitują światło o szczególnych własnościach. Powstały tomografy, których działanie opiera się na własnościach fizycznych jądra atomowego.
Dziś o atomach wiemy bardzo dużo, znamy ich właściwości. Potrafimy nawet złapać pojedynczy atomy. Wiemy, że większość masy atomu skupiona jest w jądrze, a pomiędzy jądrem a krążącymi wokół niego elektronami znajduje się pusta przestrzeń. Atomy łączą się, tworząc trwałe cząsteczki i ciała stałe. Tworzą one nasz realny świat i pozostały niezmienione od czasu jego powstania [6].
Autor: Ada Umińska
Literatura:
[1] Department of Chemistry Le Moyne College. Elements and atoms: Chapter
3, lavoisier’s elements of chemisty on-line.
[2] Biografia J. J. Thompsona Fundacja Noblowska.
[3] Biografia E. Rutherforda Fundacja Noblowska.
[4] Biografia N. Bohra Fundacja Noblowska.
[5] Wikipedia.
[6] Jearl Walker David Halliday, Robert Resnick. Podstawy Fizyki część 5. Wydawnictwo
Naukowe PWN, 2005.
Jak podobał Wam się artykuł? Oceńcie sami! Zachęcamy do wypełnienia naszej sondy!
ARTYKUŁ DO POBRANIA: Laboratoria.net - Dzień dobry, mam na imię Atom.
25 maja 2018 roku zacznie obowiązywać Rozporządzenie Parlamentu Europejskiego i Rady (UE) 2016/679 z dnia 27 kwietnia 2016 r (RODO). Potrzebujemy Twojej zgody na przetwarzanie Twoich danych osobowych przechowywanych w plikach cookies. Poniżej znajdziesz pełny zakres informacji na ten temat.
Zgadzam się na przechowywanie na urządzeniu, z którego korzystam tzw. plików cookies oraz na przetwarzanie moich danych osobowych pozostawianych w czasie korzystania przeze mnie ze strony internetowej Laboratoria.net w celach marketingowych, w tym na profilowanie i w celach analitycznych.
Administratorami Twoich danych będziemy my: Portal Laboratoria.net z siedzibą w Krakowie (Grupa INTS ul. Czerwone Maki 55/25 30-392 Kraków).
Chodzi o dane osobowe, które są zbierane w ramach korzystania przez Ciebie z naszych usług w tym zapisywanych w plikach cookies.
Przetwarzamy te dane w celach opisanych w polityce prywatności, między innymi aby:
dopasować treści stron i ich tematykę, w tym tematykę ukazujących się tam materiałów do Twoich zainteresowań,
dokonywać pomiarów, które pozwalają nam udoskonalać nasze usługi i sprawić, że będą maksymalnie odpowiadać Twoim potrzebom,
pokazywać Ci reklamy dopasowane do Twoich potrzeb i zainteresowań.
Zgodnie z obowiązującym prawem Twoje dane możemy przekazywać podmiotom przetwarzającym je na nasze zlecenie, np. agencjom marketingowym, podwykonawcom naszych usług oraz podmiotom uprawnionym do uzyskania danych na podstawie obowiązującego prawa np. sądom lub organom ścigania – oczywiście tylko gdy wystąpią z żądaniem w oparciu o stosowną podstawę prawną.
Masz między innymi prawo do żądania dostępu do danych, sprostowania, usunięcia lub ograniczenia ich przetwarzania. Możesz także wycofać zgodę na przetwarzanie danych osobowych, zgłosić sprzeciw oraz skorzystać z innych praw.
Każde przetwarzanie Twoich danych musi być oparte na właściwej, zgodnej z obowiązującymi przepisami, podstawie prawnej. Podstawą prawną przetwarzania Twoich danych w celu świadczenia usług, w tym dopasowywania ich do Twoich zainteresowań, analizowania ich i udoskonalania oraz zapewniania ich bezpieczeństwa jest niezbędność do wykonania umów o ich świadczenie (tymi umowami są zazwyczaj regulaminy lub podobne dokumenty dostępne w usługach, z których korzystasz). Taką podstawą prawną dla pomiarów statystycznych i marketingu własnego administratorów jest tzw. uzasadniony interes administratora. Przetwarzanie Twoich danych w celach marketingowych podmiotów trzecich będzie odbywać się na podstawie Twojej dobrowolnej zgody.
Dlatego też proszę zaznacz przycisk "zgadzam się" jeżeli zgadzasz się na przetwarzanie Twoich danych osobowych zbieranych w ramach korzystania przez ze mnie z portalu *Laboratoria.net, udostępnianych zarówno w wersji "desktop", jak i "mobile", w tym także zbieranych w tzw. plikach cookies. Wyrażenie zgody jest dobrowolne i możesz ją w dowolnym momencie wycofać.
Więcej w naszej POLITYCE PRYWATNOŚCI
Recenzje