- Biochemia
- Biofizyka
- Biologia
- Biologia molekularna
- Biotechnologia
- Chemia
- Chemia analityczna
- Chemia nieorganiczna
- Chemia fizyczna
- Chemia organiczna
- Diagnostyka medyczna
- Ekologia
- Farmakologia
- Fizyka
- Inżynieria środowiskowa
- Medycyna
- Mikrobiologia
- Technologia chemiczna
- Zarządzanie projektami
- Badania kliniczne i przedkliniczne
Dehydrogenaza mleczanowa (LDH): badanie właściwości enzymu oraz znaczenie diagnostyczne różnych izoform LDH, cz.I
 Dehydrogenaza mleczanowa (określana w skrócie jako LDH) jest enzymem, który katalizuje konwersję mleczanu do pirogronianu (w obecności związku NAD+) i odwrotnie (pirogronian do mleczanu w obecności NADH). Jest to enzym występujący we wszystkich komórkach oraz płynach ustrojowych [1].
Dehydrogenaza mleczanowa (określana w skrócie jako LDH) jest enzymem, który katalizuje konwersję mleczanu do pirogronianu (w obecności związku NAD+) i odwrotnie (pirogronian do mleczanu w obecności NADH). Jest to enzym występujący we wszystkich komórkach oraz płynach ustrojowych [1]. Wzrost aktywności dehydrogenazy (LDH) obserwuje się we wszystkich stanach chorobowych, które przebiegają z martwicą tkanek. Aktywność enzymu wzrasta w ostrym uszkodzeniu mięśnia sercowego, krwinek czerwonych, nerek, a także mięśni szkieletowych, wątroby, płuc oraz w uszkodzeniach skóry. Ponadto, znaczny wzrosty aktywności obserwuje się także w niedokrwistościach hemolitycznych, w niedokrwistościach spowodowanych niedoborem witaminy B2 lub kwasu foliowego, oraz w schorzeniu określanym mianem policytemii prawdziwej.
W przypadku, gdy obserwuje sie wahające wzrosty oraz spadki aktywności enzymu LDH, można wnioskować o zawale mięśnia sercowego. W pierwszych 3—4 dniach wzrost enzymu z następczym spadkiem w kolejnych 5—7 dniach choroby, może być dowodem potwierdzającym zawał serca (po wcześniejszym wykluczeniu następujących chorób: zawału płuc, choroby nowotworowej i niedokrwistości megalobiastycznej) [1].
Budowa dehydrogenazy mleczanowej (LDH)
Znaczenie diagnostyczne określania poziomu dehydrogenazy mleczanowej
Aktualnie, pewne znaczenie diagnostyczne ma LDH-C4, obecny w płynie nasiennym mężczyzn z oligospermią. W wyniku przeprowadzonych obserwacji zauważono, że pacjenci, którzy poddani zostali terapii testosteronowej i odpowiadających pozytywnie na tę terapię, wykazują wzrost aktywności LDH-C4 przed wzrostem plemników. Takie wyniki pozwalają na wyselekcjonowanie grupy osób, u których zastosowana terapia może przebiec pozytywnie i zakończyć się sukcesem terapeutycznym.
Wysoka aktywność enzymu u osób z azoospermią, może być przesłanką skłaniającą do wdrożenia terapii hormonalnej, która może również zakończyć sie pozytywnie [2]. W diagnostyce zapalenia wątroby obserwuje się wzrost w surowicy frakcji LDH5. Ponadto, wartości enzymu mierzy się także w takich chorobach jak: białaczki, nowotwory, anemie i inne, co wskazuje na duże znaczenie diagnostyczne [3].
Test optyczny Warburga
Zmiany absorbancji obserwowane w jednostce czasu będące miarą szybkości zachodzenia reakcji, która to jest proporcjonalna ( w określonych warunkach) do stężenia danego enzymu, określana jest mianem tzw. testu optycznego Warburga. Test ten często wykorzystywany jest do określania aktywności m.in. dehydrogenazy mleczanowej (LDH), oraz innych dehydrogenaz, których koenzymem jest albo NAD+ albo NADP+. Ponadto, można go także wykorzystać do oznaczania enzymów, które katalizują reakcje sprzężone z dehydrogenazami (takie, gdzie w końcowym etapie reakcji dochodzi do redukcji nukleotydów pirydynowych) [3].
Oznaczanie LDH w surowicy z wykorzystaniem metody Wróblewskiego i La Due
Wykonanie:
A ∙ 1000/ a
gdzie:
A - Średnia zmierzona wartośc absorbancji (∆A) w ciągu 1 minuty
a - Ilość (ml) surowicy użytej do wykonania oznaczenia
Aktywność LDH [U]= A ∙ (1000/0,1) / 2,07 = A ∙ 4830
A - Zmierzona średnia wartość ∆A w ciągu 1 minuty dla 0,1 ml surowicy [3].
- H4(LDH-1)
- H3M1 (LDH-2)
- H2M2 (LDH-3)
- H3M3 (LDH-4)
- M4 (LDH-5)
Obszary największej koncentracji dla każdego typu izoenzymu są następujące:
- LDH-1: serce i czerwone krwinki
- LDH-2: białe krwinki
- LDH-3: płuca
- LDH-4: nerki, łożysko, trzustka
- LDH-5: wątroba, mięśnie szkieletowe [6].
Elektroforetyczny rozdział izoenzymów LDH
Dehydrogenaza mleczanowa (LDH) przekształca mleczan do pirogronianu w trakcie odwracalnej reakcji. Enzym ten powszechnie występuje w błonach komórkowych oraz w cytoplazmie, i uwalniany jest z komórek do supernatantu hodowli natychmiast po uszkodzeniu komórek [5]. LDH stosowana jest jako marker zwyrodnienia komórek w wielu dziedzinach, m.in. w toksykologii i immunologii nowotworów. Pomiaru aktywności enzymu dokonuje się przez wykrywanie poziomu dinukleotydu nikotynamidoadeninowego (NAD+) z wykorzystaniem światła ultrafioletowego[5].
Zdjęcie: Budowa NAD, [7].
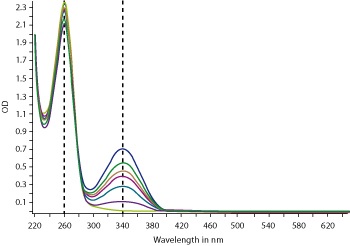
Zdjęcie: Widmo absorpcyjne dla NAD+ i NADH. NAD+- linia niebieska, NADH- linia czerwona, [10].
Test LDH
LDH zaliczana jest do enzymów cytozolowym co znaczy, że w warunkach fizjologicznych enzym ten nie jest uwalniany do środowiska, dopiero uszkodzenie mechaniczne błony plazmatycznej komórki bądź śmierć komórki spowodowana zadziałaniem czynników szkodliwych (np. działanie substancji chemicznych, czynników fizycznych), powoduje, że enzym uwalniany jest z komórek do środowiska [12].
Oznaczenie aktywności dehydrogenazy mleczanowej w supernatancie jest miarą toksyczności badanej substancji względem komórek w hodowli, ponieważ enzym ten uwalniany jest z komórek w wyniku ich uszkodzeń. Reakcje enzymatyczne w trakcie oznaczenia zachodzi w 2 etapach:
Zazwyczaj test LDH przeprowadza się z krwi, aczkolwiek można w tym celu użyć także próbkę moczu lub płynu mózgowo-rdzeniowego. W przypadku dorosłych krew do testu pobierana jest z żyły wewnętrznej łokcia lub z grzbietu dłoni. Stosowanie niektórych leków lub zażywanie narkotyków mogą powodować nieprawidłowości w wynikach. Kwas askorbinowy (witamina C) może wpływać na obniżenie poziomu LDH, zaś alkohol, leki znieczulające czy aspiryna mogą podnosić aktywność LDH. Podwyższony poziom LDH może wskazywać na wystąpienie wielu różnych chorób, w tym m.in. : nowotworów, zapalenie trzustki, mononukleazy zakaźnej czy niedokrwistość hemolityczną.
Wysoki poziom LDH wskazuje na uszkodzenie tkanki. Wysokie poziomy więcej niż jednego izoenzymu LDH mogą wskazywać na więcej niż jedną przyczynę uszkodzenia tkanki, zaś gdy poziom wszystkich pięciu izoenzymów LDH jest wysoki, może to świadczyć o niewydolności wielonarządowej [13].
Normalny stosunek LHD-1/LDH-2 jest powszechnie uważany za wiarygodny dowód na nie występowanie zawału serca . Niski poziom LDH zazwyczaj nie stanowi problemu, w większości diagnozuje się go u osób, które zażywają duże dawki witaminy C i diagnozowany jest bardzo rzadko Ponadto, znane są dwa rodzaje mutacji, które powodują obniżenie poziomu tego enzymu: pierwszy rodzaj mutacji powoduje, że osoby z daną mutacją odczuwają zmęczenie i ból mięśni, podczas gdy drugi rodzaj mutacji u ludzi jest bezobjawowy [13].
Szybkośc reakcji enzymatycznej
Oznaczanie aktywności enzymu wymaga określenia w preparacie szybkości początkowej w warunkach pełnego wysycenia tzn. przy takim stężeniu substratu, które będzie znacznie przekraczać wartość stałej Michaelisa dla danego enzymu [15].
Oznaczanie aktywności LDH
Do wykonania oznaczenia aktywności enzymu (LDH) należy użyć mieszaniny reakcyjnej w skład, której wchodzi: 40 mM bufor Tris-HCl o pH= 7.5, 25 mM KCl, 6mM EGTA zapobiega interakcji z jonami wapnia (25 ml roztworu) [15], [16].
Autor: Lidia Koperwas
Literatura:
[2]. Szutowicz A., Raszei-Szpecht A., 2009. Diagnostyka laboratoryjna. Tom I.Gdański Uniwersytet Medyczny, Zlecenie KW/224/09.Recenzent prof. dr hab.Wiesława Łysiak-Szydłowska. S. 62-63
[3]. Kłyszejko-Stefanowicz L, 2003. Ćwiczenia z biochemii. Wydawnictwo Naukowe PWN, 2003, s.529-531
[4].http://biochemistry.sote.hu/uploads/obi_okt_gra_en/obi_e_tananyag_en/obi_okt_gyakorlatok_en/obi_gya_en_LDH.pdf
[6]. http://www.healthline.com/health/lactate-dehydrogenase-test#LDHIsoenzymes
[7]. http://pubchem.ncbi.nlm.nih.gov/summary/summary.cgi?cid=5892#itabs-2d
[8]. http://analiza.ovh.org/cw/cw2.pdf
[9]. http://pchba.amu.edu.pl/cw%20Fak/cw2.pdf
[10]. Dell E.J., Detection of NADH and NADPH with the Omega’s High Speed, Full UV/Vis Absorbance Spectrometer , BMG LABTECH, Inc., Durham, USA. http://www.bmglabtech.com/application-notes/absorbance/spectrometer-nadh-nadph-170.cfm , http://www.bmglabtech.com/db_assets/applications/downloads/applications/170-nadh-nadph.pdf
[11]. Ying W., 2008. NAD+/NADH and NADP+/NADPH in cellular functions and cell death: regulation and biological consequences. Antioxid Redox Signal. 2008 Feb;10(2):179-206. Department of Neurology, University of California at San Francisco, San Francisco, California 94121, USA.
[12]. http://www.uj.edu.pl/documents/2387936/4117775/cw8.pdf
[13].http://www.healthline.com/health/lactate-dehydrogenase-test#HighLDHLevels
[14]. Hames D.B, Hooper N.M, 2007. Biochemia-krótkie wykłady. Wydanie II, Wydawnictwo Naukowe PAN 2007, s.96-100
[15]. Bryła J., Drożak J., Garstka M., Jagielski A., Jarzyna R., Kiersztan A., Kaniuga Z., Winiarska K., 2011. Enzymologia I, s. 20-25. Materiały do ćwiczeń dla studentów kierunku Biotechnologia Wydziału Biologii UW. Skrypt przygotowany przez pracowników Zakładu Regulacji Metabolizmu,Instytut Biochemii Wydziału biologii. http://www.biol.uw.edu.pl/zrm/Skrypty/2011EnzymI.pdf
[16]. http://www.wiener-lab.com.ar/wiener/catalogo/archivos/7702_mg_color_aa_pl.pdf
[17]. BIELLMANN J.F., SAMAMA J.P., BRANDEN C.I., EKLUND H., 1979. X-Ray Studies of the Binding of Cibacron Blue F3GA to Liver Alcohol Dehydrogenase. Eur.
J. Biochem. 102, 107-110 (1979). http://onlinelibrary.wiley.com/doi/10.1111/j.1432-1033.1979.tb06268.x/pdf
[18]. Angal S., Dean P.D.G., 1977. The Effect of Matrix on the Binding of Albumin to Immobilized Cibacron Blue. Biochem J.(1997) 167, 301-303, http://www.docstoc.com/docs/28020884/Immobilized-Cibacron-Blue
[19]. http://www.biofizyka.p.lodz.pl/ch8.pdf
[20]. Drent M., Cobben N.A.M., Herderson R.F., Wouters E.F.M., van Dieijen-Visser M., 1996. Usefulness of lactate dehydrogenase and its isoenzymes as indicators of lung damage or inflammation. Eur Respir J, 1996, 9, 1736–1742 DOI: 10.1183/09031936.96.09081736. http://erj.ersjournals.com/content/9/8/1736.full.pdf
[21].http://www.laboklin.de/pdf/pl/wetinfo/aktualnosci/2012_01_analizy_wysiekow_oplucnowych.pdf
[22]. Sigma- Aldrich, In Vitro Toxicology Assay Kit, Lactic Dehydrogenase based. Technical Bulletyn, http://www.sigmaaldrich.com/etc/medialib/docs/Sigma/Bulletin/tox7bul.Par.0001.File.tmp/tox7bul.pdf
[23]. http://www.e-biotechnologia.pl/Artykuly/glikoliza/
[24]. Al-Saadoon E.A., MRCP (Pead)* Al-Naama L.M, Hassan J.K., 2003. Serum Lactate Dehydrogenase (LDH) Activity in Children with Malignant Diseases. Bahrain Medical Bulletin, Vol.25, No. 2, June 2003, http://www.bahrainmedicalbulletin.com/june_2003/Serum.pdf
[25]. Baba Ch., Yanagida K., Kanzaki T., Baba M., 2005. Colorimetric lactate dehydrogenase (LDH) assay for evaluation of antiviral activity against bovine viral diarrhoea virus (BVDV) in vitro. Antiviral Chemistry & Chemotherapy 16:33–39. ©2005 International Medical Press










Recenzje